T ℃时在2 L密闭容器中使X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的物质的量变化如图1所示;若保持其他条件不变,温度分别为T1和T2时,Y的百分含量与时间的关系如图2所示。则下列结论正确的是( )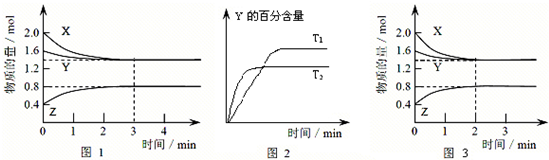
| A.反应进行的前3 min内,用X表示的反应速率v(X)=0.3 mol·L-1·min-1 |
| B.容器中发生的反应可表示为:3X(g)+Y(g) =2Z(g) |
| C.保持其他条件不变,升高温度,反应的化学平衡常数K增大 |
| D.若改变反应条件,使反应进程如图3所示,则改变的条件是增大压强 |
A、B为同主族的两元素,A在B的上一周期,若A的原子序数为n,则B的原子序数不
可能为
A.n+8 B.n+18 C.n+20 D.n+32
下列关于元素周期表的说法正确的是
| A.能生成碱的金属元素都在ⅠA族 |
| B.原子序数为14的元素位于元素周期表的第3周期ⅣA族 |
| C.稀有气体元素原子的最外层电子数均为8 |
| D.第二周期ⅣA族元素的原子核电荷数和中子数都一定为6 |
下列化学用语正确的是
A.CO2的电子式: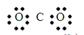 |
B.Mg2+的结构示意图: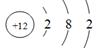 |
C.Na2O的电子式: Na+2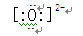 |
D.N2的结构式:N≡N |
X元素最高氧化物对应的水化物为H3XO4,则它对应的气态氢化物为
| A.HX | B.H2X | C.XH4 | D.XH3 |
甲、乙是同周期的非金属元素,若原子序数甲小于乙,则下列四种叙述中正确的是
| A.气态氢化物的稳定性甲比乙弱 | B.最高价氧化物的水化物的酸性甲比乙强 |
| C.阴离子的还原性甲比乙弱 | D.金属性甲比乙弱 |