一定条件下,可逆反应2X(g)+3Y(g) 4Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),平衡时X、Y、Z的浓度分别为0.2mol·L-1、0.3 mol·L-1、0.16 mol·L-1,则下列判断不合理的是
4Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),平衡时X、Y、Z的浓度分别为0.2mol·L-1、0.3 mol·L-1、0.16 mol·L-1,则下列判断不合理的是
| A.c1∶c2=2∶3 |
| B.X、Y的转化率不相等 |
| C.平衡时,Y和Z的生成速率之比为3∶4 |
| D.c1的取值范围为0<c1<0.28 mol·L-1 |
下列溶液中,跟100mL 0.5mol/L NaCl溶液所含的Cl-物质的量浓度相同的是()
| A.100mL 0.5mol/L MgCl2溶液 | B.200mL 0.25mol/L AlCl3溶液 |
| C.50ml 1mol/L NaCl溶液 | D.25ml 0.5mol/L HCl溶液 |
为使人们确知含碘物质的存在,研究性学习小组同学设计了一种简便的检验方法,利用该物质在酸性条件下与KI反应有单质碘生成的性质,选用下列生活常见的物质就可完成。请你从下列物质中选出合适的一组()
①自来水 ②食醋 ③淀粉 ④食糖 ⑤碘化钾试纸 ⑥碘酒
| A.①③④⑤ | B.②③④⑤ | C.①③⑤⑥ | D.①②③⑤ |
设NA表示阿伏加德罗常数的值,下列说法正确的是()
| A.NA个氧气分子与NA个氖气分子的质量比是4∶5 |
| B.17gOH-与19gH3O+所含电子数相等 |
| C.14g14C和12g12C所含的中子数相等 |
| D.标准状况下,11.2LCO2与常温常压下8.5gNH3所含分子数相等 |
下列说法正确的是(N0表示阿伏加德罗常数的数值)()
| A.在常温常压下,11.2 L N2含有的分子数为0.5 N0 |
| B.在常温常压下,1 mol Ne含有的原子数为N0 |
| C.71 g Cl2所含原子数为2N0 |
| D.在同温同压时,相同体积的任何气体单质所含的原子数相同 |
下列关于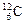 、
、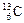 、
、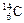 的说法正确的是()
的说法正确的是()
| A.它们的化学性质相似 | B.它们是碳元素的三种同位素 |
| C.它们是碳元素的三种单质 | D.它们是碳元素的同素异形体 |