亚氯酸钠(NaClO2)主要用于棉纺、造纸业的漂白剂,也用于食品消毒、水处理等,亚氯酸钠受热易分解。以氯酸钠等为原料制备亚氯酸钠的工艺流程如下: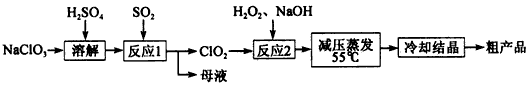
(1)提高“反应l”反应速率的措施有______________(写出一条即可)。
(2)“反应2”的氧化剂是________,该反应的化学方程式为__________。
(3)采取“减压蒸发”而不用“常压蒸发”,原因是__________________。
(4)从 “母液”中可回收的主要物质是__________________________。
(5)“冷却结晶”后经_____________(填操作名称)即可获得粗产品。
在下列物质中:①K2SO4、②HCHO、③MgSO4、④Hg(NO3)2、⑤NH4Cl、⑥KOH,能使蛋白质变性的是________,能使蛋白质发生盐析的是________。
现有通式为(CH2O)n的六种有机物,性质如下:
①甲是无色有刺激性气味的气体,可以发生银镜反应;
②乙、丙、丁的相对分子质量均为甲的2倍,戊的相对分子质量是甲的3倍,己的相对分子质量是甲的6倍;
③乙、戊的水溶液可使紫色石蕊试液变红,还可以与乙醇在一定条件下酯化,乙和戊之间也能酯化;
④戊结构中含有—CH3,两分子戊可形成环状酯;
⑤丙不溶于水;丁、己两种物质的水溶液均呈中性;丙既能水解,又能发生银镜反应;丁能与钠反应放出H2,且能与新制Cu(OH)2悬浊液加热反应产生红色沉淀;己能发生银镜反应,它可由淀粉水解制得。
(1)推断各物质的结构,写出其结构简式。
甲________,乙________,丙________,
丁________,戊________,己________。
(2)甲~己中能与NaOH溶液反应的是________,(填序号,下同)能发生酯化反应的是________,能被H2还原为醇的是________,能发生银镜反应的是________。
某厂以甘蔗为原料制糖,对产生的大量甘蔗渣按下图所示转化进行综合利用。其中B是A水解的最终产物;C的化学式为C3H6O3,一定条件下2个C分子间脱去2个水分子可生成一种六元环状化合物;D可使溴水褪色;F是具有香味的液体。(图中部分反应条件及产物没有列出)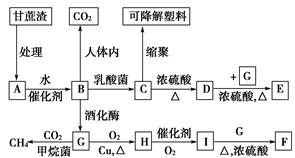
回答下列问题:
(1)A的名称是________,F的结构简式__________,
D的结构简式________。
(2)C→D的反应类型为________。D→E的反应类型为________。
(3)写出下列反应的方程式:
A→B:______________________________;
G→H:______________________________________。
(4)H分子所含官能团的名称是________,实验室中常用于检验该官能团的试剂的名称是(只写一种)_____________________________。
分别取1 mol葡萄糖进行下列实验:
(1)银镜反应时,需银氨络合离子________mol,反应后葡萄糖变为________,其结构简式是_________________________。
(2)与乙酸反应生成酯,从理论上讲完全酯化需要________g乙酸。
(3)若使之完全转化为CO2和H2O,所需氧气的体积在标准状况下为________L,反应的方程式是__________________________。
将蔗糖溶于水配成10%的溶液,分装在两支试管中。分别进行如下实验:
(1)在第一支试管中加入新制Cu(OH)2悬浊液并加热,没有红色沉淀产生,原因是____________________________;
(2)在第二个试管中加入几滴稀硫酸,再放在水浴中加热,再加入足量NaOH并加入新制Cu(OH)2悬浊液,加热。
①现象是__________________________;
②原因是__________________________;
③加入足量NaOH的作用是________________________;
④上述实验中发生的化学方程式是__________________。