工业上由铝土矿(主要成分是Al2O3和Fe2O3)和焦炭制备无水AlCl3的流程如下: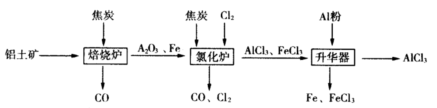
已知:AlCl3,FeCl3,分别在183℃、315℃升华
(1)在焙烧炉中发生反应:
①Fe2O3(s)+3C(s) 2Fe(s)+3CO(g) △H=-492.7kJ/mol
2Fe(s)+3CO(g) △H=-492.7kJ/mol
②3CO(g)+ Fe2O3(s) 2Fe(s)+3CO2(g) △H=+25.2kJ/mol
2Fe(s)+3CO2(g) △H=+25.2kJ/mol
反应2Fe2O3(s)+3C(s) 4Fe(s)+3CO2(g) △H=___________kJ/mol。
4Fe(s)+3CO2(g) △H=___________kJ/mol。
(2)①Al2O3,Cl2和C在氯化炉中高温下发生反应,当生成1molAlCl3时转移______mol电子;炉气中含有大量CO和少量Cl2,可用Na2SO3溶液除去Cl2,其离子方程式为_______。在温度约为700℃向升华器中加入铝粉,发生反应的化学方程式为 。充分反应后温度降至_____以下(填“183℃、315℃之一),开始分离收集AlCl3。
②将AlCl3· 6H2O溶于浓硫酸进行蒸馏,也能得到一定量的无水AlCl3,此原理是利用浓硫酸下列性质中的 (填字母序号)。
①氧化性 ②吸水性 ③难挥发性 ④脱水性
a.只有① b.只有② c.只有②③ d.只有②③④
(3)海洋灯塔电池是利用铝、石墨为电极材料,海水为电解质溶液,构成电池的其正极反应式________,与铅蓄电池相比.释放相同电量时,所消耗金属电极材料的质量比m(Al): m(Pb)=__________________。
(9分)(1)在标准状况下,①6.72 L CH4气体;②3.01×1023个 HCl气体分子;③13.6 g H2S气体;④0.2 mol NH3,下列对这四种气体所含分子物质的量的关系从小到大的排列是(用上述数字序号表示)_______ ______________________________。
(2)粗盐经提纯后得到NaCl溶液,再经蒸发、结晶、烘干得精盐。
①蒸发操作中使用到的仪器除铁架台(带铁圈)外,还需要的仪器名称为(写出三种)_________________。
②该同学将所得精盐配成溶液,用于另一实验:实验中需要用60 mL 2 mol/L的NaCl溶液,配制过程中用托盘天平称取的精盐质量为________,该同学将精盐放在天平的右盘中称量好后,配制成溶液,则该溶液的浓度________2 mol·L-1(填“>”、“<”或“=”)。
(8分)某溶液中可能含有Ba2+、K+、Na+、SO42-、CO32-、HCO3-、Cl-、Br-等离子中的两种或几种。现进行以下实验:
①取上述溶液少量加入过量BaCl2溶液,产生白色沉淀,过滤,向沉淀中加入过量的硝酸,沉淀完全溶解,并产生气体;
②向实验①的滤液中滴入AgNO3溶液,出现淡黄色沉淀;
③取原溶液进行焰色反应,直接观察,火焰呈黄色。
由以上实验判断,该溶液中肯定存在的离子有_________________________;肯定不存在的离子
为___________________;不能确定是否存在的离子为________________________。
如下图所示的装置, C、D、E、F都是惰性电极。将电源接通后,向乙中滴入酚酞液,在F极附近显红色。试回答以下问题:
(1)电源的A极是_______;
(2)写出甲装置中电解反应的总方程式: _________;
(3)如果收集乙装置中产生的气体,EF两电极产生的气体的体积比是______________;
(4)欲用丙装置给铜镀银,G应该是_______,电镀液的主要成分是_________(填化学式)。
在一定条件下A与B反应可生成C和D,其能量变化如图: 
(1)下列有关反应A+B===C+D的说法正确的是。
| A.反应前后原子的种类和数目一定不变 |
| B.该反应若有能量变化,则一定是氧化还原反应 |
| C.该反应若为放热反应,则不需加热反应就一定能自发进行 |
| D.反应物的总质量与生成物的总质量一定相等,且遵循能量守恒 |
(2)若E1<E2,则生成物的总能量(填“>”、“<”或“=”)反应物的总能量,为_(填“吸热”或“放热”)反应。
用碳棒作电极,在H+、Na+、Cu2+、Ag+、Cl-、NO3-、SO42-等离子中选出适当离子组成电解质,电解其溶液,写出符合条件的一种电解质的化学式:
(1)当阴极放出H2,阳极放出O2时,电解质是;
(2)当阴极析出金属,阳极放出O2时,电解质是;
(3)当阴极放出H2,阳极放出Cl2时,电解质是;
(4)通过电子的物质的量与阴极析出的金属、阳极析出的气体的物质的量之比为4∶2∶1时,电解质的化学式是。