某校化学兴趣小组设计了图示实验装置(图中省略了夹持仪器)来测定某铁碳合金中铁的质量分数,并探究铁与浓硫酸的反应。
(1)m克铁碳合金中加入过量浓硫酸,未点燃酒精灯前,A、B均无明显现象,其原因是①常温下碳与浓硫酸不反应;② 。
(2)写出加热时A中碳与浓硫酸发生反应的化学方程式 。
(3)B中的现象是 ;C的作用是 。
(4)随着反应的进行,A中还可能发生某些离子反应,写出相应的离子方程式
反应一段时间后,从A中逸出气体的速率仍然较快,除因温度较高,反应放热外,还可能的原因是 ;
(5)待A中不再逸出气体时,停止加热,拆下E并称重,E增重bg。则铁碳合金中铁的质量分数为 (写含m、b的表达式)。
(6)某同学认为上述方法较复杂,使用下图所示的装置和其它常用实验仪器测定某些数据即可。为了快速和准确的计算出铁的质量分数,最简便的实验操作是 (填写代号)。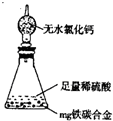
A.用排水法测定H2的体积
B.反应结束后,过滤、洗涤、称量残渣的质量
C.测定反应前后装置和药品的总质量
下图所示为某化学兴趣小组设计的乙醇催化氧化的实验装置(图中加热仪器、铁架台、铁夹等均未画出)。图中A试管盛有无水乙醇(沸点为78℃),B处为螺旋状的细铜丝,C处为无水硫酸铜粉末,干燥管D中盛有碱石灰,E为新制的氢氧化铜,F为氧气的发生装置。
(1)在实验过程中,需要加热的仪器(或区域)有(填仪器或区域的代号A~F)________。
(2)B处发生的化学反应方程式为________________________________________。
(3)C处应出现的现象是_________________________________________________,
D处使用碱石灰的作用是_____________________________________________,
E处应出现的实验现象是 ____________________________________________,
F处可以添加的固体药品是 __________________________________________。
(4)若本实验中拿去F装置(包括其上附的单孔塞和导管),同时将A试管处原来的双孔塞换成单孔塞用以保证装置的气密性,其它操作不变,则发现C处无明显变化,而E处除了依然有上述(3)中所出现的现象之外,还有气体不断地逸出。由此推断此时B处发生反应的化学方程式为___________。
除去工业尾气中的氮氧化物,常用氨催化吸收法。原理是NH3与NOx反应生成无毒物质。某同学采用以下装置和步骤模拟工业上氮氧化物的处理过程。
(一)提供的装置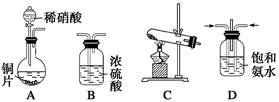
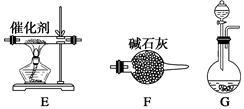
(二)NH3的制取
(1)下列有关实验室制备气体的说法正确的有(填序号)。
①用赤热的炭与水蒸气反应制取氢气
②用排饱和食盐水的方法收集氯气
③实验室制氧气有时需要加热,有时不需要加热
④用无水氯化钙干燥氨气
(2)若选择装置G制取氨气,则分液漏斗中盛装的液体试剂是。
(3)若选择装置C制取氨气,则反应的化学方程式是。
(三)模拟尾气的处理
选用上述部分装置,按下列顺序连接成模拟尾气处理装置,回答有关问题: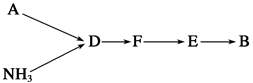
(4)A装置中反应的离子方程式为__________________________________。
(5)D装置中的液体可换成(填序号)。
a. CuSO4b. H2O c. CCl4d. 浓硫酸
(6)该同学所设计的模拟尾气处理实验存在的明显缺陷是__________________。
某品牌糖衣片补血剂,除去糖衣后显淡蓝绿色,主要成分是硫酸亚铁,不含其它铁的化合物。某研究性学习小组为测定该补血剂中硫酸亚铁的含量进行了以下探究:
请回答下列问题:
Ⅰ.(1)实验时用10mol·L-1的浓硫酸配制100 mL 1 mol·L-1 H2SO4溶液,所需浓硫酸的体积为mL。
(2)容量瓶所具备的功能是(填序号)。
A.配制一定体积准确浓度的溶液
B.长期贮存溶液
C.常用来代替量筒量取一定体积的液体
D.用来溶解固体溶质
(3)在下列配制过程示意图中,错误的有(填序号)。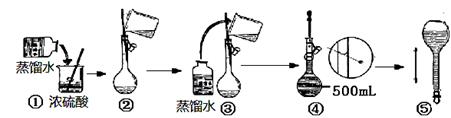
(4)下列说法正确的是。
A.洗涤烧杯2~3次,并将洗涤液移入容量瓶以减少误差
B.某同学将浓硫酸稀释后未冷却至室温便将溶液转移至容量瓶,所配溶液浓度会偏低
C.定容时仰视观察, 所配溶液浓度会偏低
Ⅱ.(1)步骤③中产生的红褐色物质是(填化学式)。
(2)从红褐色的悬浊液到最后的称量,其过程中所需的基本操作为:
a., b.洗涤, c.灼烧, d.冷却
(3)若称得固体的质量为ag,则每片补血剂中含硫酸亚铁的质量为g。
用苯甲醛制备苯甲醇和苯甲酸,已知反应原理: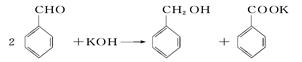
苯甲醛易被空气氧化;苯甲酸的熔点121.7℃,沸点249℃,溶解度0.34g(常温);苯甲醇的沸点为205.3℃;乙醚的沸点34.8℃,难溶于水。
制备苯甲醇和苯甲酸的主要过程如下: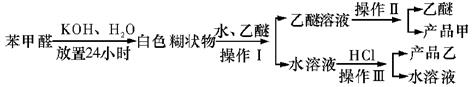
(1)混合苯甲醛、氢氧化钾和水应选用的仪器是(填序号)。
A.容量瓶 B.烧杯 C.带胶塞的锥形瓶
(2)操作II的名称是,产品甲的成分是。
(3)操作III的名称是,产品乙是。
海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验: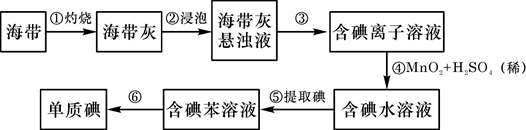
请填写下列空白:
(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是()
(从下列仪器中选出所需的仪器,用标号字母填写在空白处)。
| A.烧杯 |
| B.坩埚 |
| C.表面皿 |
| D.泥三角 |
E.酒精灯
F.干燥器
(2)步骤⑤的仪器名称是;
(3)步骤⑥的目的是从含碘的苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是。
(4)若反应后有Mn2+步骤④反应的离子方程式是。
(5)步骤⑤中,某学生选择用苯来提取碘的理由是。