某品牌糖衣片补血剂,除去糖衣后显淡蓝绿色,主要成分是硫酸亚铁,不含其它铁的化合物。某研究性学习小组为测定该补血剂中硫酸亚铁的含量进行了以下探究:
请回答下列问题:
Ⅰ.(1)实验时用10mol·L-1的浓硫酸配制100 mL 1 mol·L-1 H2SO4溶液,所需浓硫酸的体积为 mL。
(2)容量瓶所具备的功能是 (填序号)。
A.配制一定体积准确浓度的溶液
B.长期贮存溶液
C.常用来代替量筒量取一定体积的液体
D.用来溶解固体溶质
(3)在下列配制过程示意图中,错误的有(填序号) 。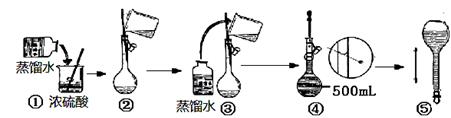
(4)下列说法正确的是 。
A.洗涤烧杯2~3次,并将洗涤液移入容量瓶以减少误差
B.某同学将浓硫酸稀释后未冷却至室温便将溶液转移至容量瓶,所配溶液浓度会偏低
C.定容时仰视观察, 所配溶液浓度会偏低
Ⅱ.(1)步骤③中产生的红褐色物质是(填化学式) 。
(2)从红褐色的悬浊液到最后的称量,其过程中所需的基本操作为:
a. , b.洗涤, c.灼烧, d.冷却
(3)若称得固体的质量为ag,则每片补血剂中含硫酸亚铁的质量为 g。
在平板电视显示屏生产过程中产生的废玻璃粉末中含有二氧化铈(CeO2).
(1)在空气中煅烧Ce(OH)CO3可制备CeO2,该反应的化学方程式
(2)已知在一定条件下,电解熔融状态的CeO2可制备Ce,写出阴极的电极反应式 ;
(3)某课题组以上述废玻璃粉末(含有SiO2、Fe2O3、CeO2以及其他少量不溶于稀酸的物质)为原料,设计如图1流程对资源进行回收,得到Ce(OH)4和硫酸铁铵.
①得到滤渣B时,需要将其表面杂质洗涤干净.洗涤的操作是 .
②反应(1)的离子方程式为 .
③操作I的名称是
④如图2,氧化还原滴定法测定制得的Ce(OH)4产品的纯度.
该产品中Ce(OH)4的质量分数为 (保留小数点后两位).若滴定所用FeSO4溶液已在空气中露置了一段时间,则测得该Ce(OH)4产品的纯度 (“偏高”、“偏低”或“无影响”).
草酸钴用途广泛,可用于指示剂和催化剂的制备。一种利用水钴矿[主要成分为Co2O3,含少量Fe2O3、Al2O3、MnO、MgO、CaO等]制取CoC2O4·2H2O工艺流程如下:
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 |
Fe(OH)3 |
Fe(OH)2 |
Co(OH)2 |
Al(OH)3 |
Mn(OH)2 |
| 完全沉淀的pH |
3.7 |
9.6 |
9.2 |
5.2 |
9.8 |
(1)浸出过程中加入Na2SO3的目的是将_____________还原(填离子符号)。
(2)NaClO3的作用是将浸出液中的Fe2+氧化成Fe3+,产物中氯元素处于最低化合价。该反应的离子方程式为____________。
(3)萃取剂对金属离子的萃取率与pH的关系如图所示。滤液Ⅱ中加入萃取剂的作用是_________;使用萃取剂适宜的pH是______。
A.接近2.0 B.接近3.0 C.接近5.0
(4)“除钙、镁”是将溶液中Ca2+与Mg2+转化为MgF2、CaF2沉淀。已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10。当加入过量NaF后,所得滤液c(Mg2+)/ c (Ca2+)= 。
甲酸(HCOOH)是一种有刺激性气味的无色液体,有很强的腐蚀性。熔点8.4℃,沸点100.7℃,能与水、乙醇互溶,加热至160℃即分解成二氧化碳和氢气。
(1)实验室可用甲酸与浓硫酸共热制备一氧化碳:HCOOH H2O+CO↑,实验的部分装置如下图所示。制备时先加热浓硫酸至80℃~90℃,再逐滴滴入甲酸。
H2O+CO↑,实验的部分装置如下图所示。制备时先加热浓硫酸至80℃~90℃,再逐滴滴入甲酸。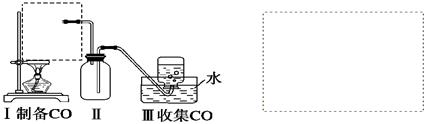
①从下图挑选所需的仪器,在虚线框中画出Ⅰ中所缺的气体发生装置(添加必要的塞子、玻璃管、胶皮管,固定装置不用画),并标明容器中的试剂。
②装置Ⅱ的作用是_____________________________________________。
(2)实验室可用甲酸制备甲酸铜。其方法是先用硫酸铜和碳酸氢钠作用制得碱式碳酸铜,然后再与甲酸制得四水甲酸铜[Cu(HCOO)2·4H2O]晶体。相关的化学方程式是:
2CuSO4+4NaHCO3===Cu(OH)2·CuCO3↓+3CO2↑+2Na2SO4+H2O
Cu(OH)2·CuCO3+4HCOOH+5H2O===2Cu(HCOO)2·4H2O+CO2↑
实验步骤如下:
I.碱式碳酸铜的制备:
①步骤ⅰ是将一定量CuSO4·5H2O晶体和NaHCO3固体一起放到研钵中研磨,其目的是___________。
②步骤ⅱ是在搅拌下将固体混合物分多次缓慢加入热水中,反应温度控制在70℃~80℃,如果看到______(填写实验现象),说明温度过高。
II.甲酸铜的制备:
将Cu(OH)2·CuCO3固体放入烧杯中,加入一定量热的蒸馏水,再逐滴加入甲酸至碱式碳酸铜恰好全部溶解,趁热过滤除去少量不溶性杂质。在通风橱中蒸发滤液至原体积的1/3时,冷却析出晶体,过滤,再用少量无水乙醇洗涤晶体2—3次,晾干,得到产品。
a、“趁热过滤”中,必须“趁热”的原因是 。
b、用乙醇洗涤晶体的目的是 。
(1)写出MnO2与浓盐酸反应制Cl2的化学方程式 。
已知KMnO4与浓盐酸在常温下反应也可制得Cl2,某同学利用该原理,用右图所示的装置制备纯净、干燥的氯气,并做氯气与金属反应的实验。每个虚线框表示一个单元装置,其中有错误的是哪几处? (填序号)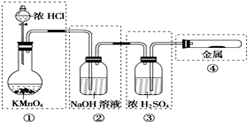
(2)化工厂生产盐酸的主要过程如图甲所示: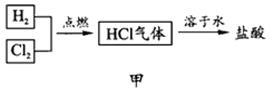
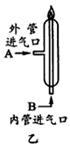
其中关键的一步为(如图乙所示)氯气和氢气在燃烧管口燃烧,生成HCl。由于氯气有毒,因此,通入气体的合理方式是:A处通入____, B处通入___,该过程涉及的操作有:①通氯气②通氢气③点燃正确的操作顺序为 (填序号)
(3)向盛有KI溶液的试管中加入少许CCl4后滴加氯水,CCl4层变成紫色。如果继续向试管中滴加氯水,振荡,CCl4层会逐渐变浅,最后变成无色。完成下列填空:
① 写出并配平CCl4层由紫色变成无色的化学反应方程式(如果化学计量数是1,也请写上):__ +__
+__ +__
+__ ―→__
―→__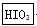 +__
+__
② 加碘盐中含碘量为20~50 mg·kg-1。制取加碘盐(含KIO3的食盐)1 000 kg,若用KI与Cl2反应制KIO3,至少需要消耗Cl2 L(标准状况,保留2位小数)
I、II两学习小组分别进行探究性的实验:
I组:为了分别研究SO2和Cl2的性质,设计了如图所示的实验装置。
(1)若从左端分别通入SO2和Cl2,则装置I中观察到的现象是否相同? (填“相同”或“不相同”);当通入SO2时,装置III中发生反应的离子方程式为 ;该反应中SO2表现出 性。
(2)若装置II中装有5.0mL 1.0×10-3mol·L-1碘水,当通入足量Cl2完全反应后,共转移了5.0×10-5mol电子,则该反应的化学方程式为 。
(3)你认为乙组设计的装置是否有不足之处? (填“有”或“无”)。如果有,请写出改进方法: (如果无,此空不答)。
II组:为了探究Cl2和SO2同时通入H2O中发生的反应,设计了如图所示的实验装置。
(1)气体发生装置A中产生的气体化学式为 。
(2)装置D中发生反应的化学方程式为 ;在装置D反应后所得溶液中加入BaCl2溶液,观察到的现象是 。
(3)装置C中饱和食盐水的作用是 ;装置E的作用是 。