下列根据实验操作和现象所得出的结论正确的是( )
| |
实验操作 |
现象 |
解释或结论 |
| A |
向溶液X中先滴加稀硝酸,再滴加Ba(NO3)2溶液 |
出现白色沉淀 |
溶液X中一定含有SO |
| B |
等体积pH=3的HA和HB 两种酸分别与足量的锌反 应,排水法收集气体 |
HA放出的氢气多且反应速率快 |
HB酸性比HA强 |
| C |
在镁、铝为电极,氢氧化钠为电解质的原电池装置中 |
镁表面有气泡 |
金属活动性:Al>Mg |
| D |
向1 mL 1%的NaOH溶液中 加入2 mL 2%的CuSO4溶 液,振荡后加入0.5 mL有 机物Y,加热 |
未出现砖红色 沉淀 |
Y中不含有醛基 |
实验室需要200 mL 1 mol·L-1的CuSO4溶液,下列有关配制该溶液的叙述,正确的是()
| A.称取32 g无水硫酸铜,加入200 mL水,在250 mL的容量瓶中配成溶液 |
| B.称取50 g CuSO4·5H2O,在250 mL的容量瓶中配成200 mL溶液 |
| C.称取40 g无水硫酸铜,加入250 mL水,在250 mL的容量瓶中配成250 mL溶液 |
| D.称取62.5 g CuSO4·5H2O,在250 mL的容量瓶中配成250 mL溶液 |
下表列出了四种溶液溶质的质量分数和物质的量浓度数值:
| 溶质 |
HCl |
HNO3 |
CH3COOH |
NaOH |
| 溶质的质 量分数/% |
36.5 |
63 |
40 |
40 |
| 物质的量浓 度/mol·L-1 |
11.8 |
13.8 |
10.6 |
14.3 |
则各溶液中密度最小的是()
| A.HCl | B.HNO3 |
| C.CH3COOH | D.NaOH |
一种硫酸溶液的浓度为c mol·L-1、密度为ρ g·cm-3,则这种溶液的质量分数为()
A.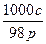 ×100% ×100% |
B.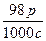 ×100% ×100% |
C.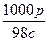 ×100% ×100% |
D. ×100% ×100% |
配制下列溶液的操作使溶液浓度偏高的是()
| A.等体积18 mol·L-1浓H2SO4和蒸馏水混合配制9 mol·L-1 H2SO4 |
| B.配制500 mL 6 mol·L-1盐酸,容量瓶未干燥就配制溶液 |
| C.配制1 mol·L-1 NaOH溶液,已定容后,再正倒摇匀,竖直后发现液面稍低于刻度线 |
| D.配制好的0.2 mol·L-1 NaCl溶液从容量瓶转移到刚用蒸馏水洗净的清洁玻璃塞细口瓶中 |
将一定量溶质的质量分数为6%的Na2CO3溶液加热蒸发掉15 g水后,还剩溶质的质量分数为14%的溶液10 mL,此时溶液的浓度为( )
| A.1.49 mol·L-1 | B.1.52 mol·L-1 |
| C.2 mol·L-1 | D.2.5 mol·L-1 |