化学与科学、技术、社会和环境密切相关。下列有关说法中错误的是
| A.对废旧电池进行回收处理,主要是为了环境保护和变废为宝 |
| B.用电解水的方法制取大量H2,可以缓解能源不足的问题 |
| C.大力开发和应用氢能源有利于实现“低碳经济” |
| D.工业上,不能采用电解MgCl2溶液的方法制取金属镁 |
将浓度为0.1mol/LHCN溶液加水不断稀释,下列各量始终保持增大的是
| A.c(H+) | B.电离平衡常数K | C. |
D. |
在一定条件下NO2与SO2气体发生反应,NO2(g)+SO2(g) SO3(g)+NO(g)ΔH=-41.8kJ·mol-1。将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是
SO3(g)+NO(g)ΔH=-41.8kJ·mol-1。将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是
| A.混合气体颜色保持不变 | B.体系压强保持不变 |
| C.SO3和NO的体积比保持不变 | D.每消耗1 mol SO3的同时生成1 mol NO2 |
已知:2H2(g)+O2(g) ="==" 2 H2O (l)△H= -571.6 kJ· mol-1,下列说法正确的是
| A.2 L液态水分解成2L氢气与1L氧气吸收571.6kJ热量 |
| B.2 mol氢气与1mol氧气反应生成2mol气态水放出热量大于571.6kJ |
| C.在相同条件下,2 mol氢气与1mol氧气的能量总和大于2mol液态水的能量 |
| D.使用催化剂能降低该反应的活化能使反应放出得热量小于571.6kJ |
反应A2(g) + 3B2(g)  4C2(g) + 2D2 (g)在5L密闭容器中进行,半分钟后,C2的物质的量增加了0.3mol,则此反应的平均速率
4C2(g) + 2D2 (g)在5L密闭容器中进行,半分钟后,C2的物质的量增加了0.3mol,则此反应的平均速率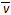 x
x
A.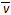 (B2) =" 0.01mol·(L·s)" –1 (B2) =" 0.01mol·(L·s)" –1 |
B.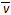 (C2) =" 0.002mol·(L·s)" –1 (C2) =" 0.002mol·(L·s)" –1 |
C.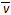 (D2) =" 0.006mol·(L·s)" –1 (D2) =" 0.006mol·(L·s)" –1 |
D.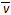 (A2) =" 0.008mol·(L·s)" –1 (A2) =" 0.008mol·(L·s)" –1 |
下列物质属于电解质的是()
①氯化钠溶液 ②氯化铵固体 ③铜 ④石墨 ⑤熔融NaOH ⑥盐酸 ⑦乙酸
⑧NH3·H2O ⑨三氧化硫
| A.①②⑥⑧ | B.②⑤⑦⑧ | C.②⑤⑥⑦ | D.②④⑤⑨ |