向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:A(g)+xB(g) 2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以下图和下表表示。下列说法正确的是
2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以下图和下表表示。下列说法正确的是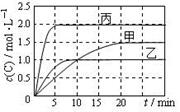
| 容器 |
甲 |
乙 |
丙 |
| 容积 |
0.5L |
0.5L |
1.0L |
| 温度/℃ |
T1 |
T2 |
T2 |
| 反应物 起始量 |
1.5molA 0.5molB |
1.5molA 0.5molB |
6.0molA 2.0molB |
A.10min内甲容器中反应的平均速率: v(A) = 0.05mol·(L·min)-1
B.由图可知T1>T2,且该反应为吸热反应
C.x=1,若平衡时保持温度不变,改变容器体积平衡不移动
D.T2℃,丙容器比乙容器反应快的原因可能是使用了催化剂
如图是乙烯分子的模型,对乙烯分子中的化学键分析正确的是
| A.sp2杂化轨道形成σ键、未杂化的2p轨道形成π键 |
| B.sp2杂化轨道形成π键、未杂化的2p轨道形成σ键 |
| C.C—H之间是sp2形成的σ键,C—C之间是未能参加杂化的2p轨道形成的π键 |
| D.C—C之间是sp2形成的σ键,C—H之间是未参加杂化的2p轨道形成的π键 |
对于原子半径的理解,不正确的是
| A.同周期元素(除了稀有气体元素外),从左到右,原子半径依次减小。 |
| B.对于第三周期元素,从钠到氯,原子半径依次减小。 |
| C.各元素的原子半径总比其离子半径大。 |
| D.阴离子的半径大于其原子半径,阳离子的半径小于其原子半径。 |
食盐晶体是由钠离子(下图中的“º”)和氯离子(下图中的“•”)组成的,且均为等距离的交错排列。已知食盐的密度是2.2 g·cm-3,阿伏加德罗常数6.02×1023 mol-1。在食盐晶体中两个距离最近的钠离子中心间的距离最接近于
| A.3.0×10-8 cm |
| B.3.5×10-8 cm |
| C.4.0×10-8 cm |
| D.5.0×10-8 cm |
下列关于金属晶体的叙述正确的是
| A.常温下,金属单质都以金属晶体形式存在 |
| B.金属离子与自由电子之间的强烈作用,在一定外力作用下,不因变形而消失 |
| C.钙的熔沸点低于钾 |
| D.温度越高,金属的导电性越好 |
下列说法正确的是
①具有规则几何外形的固体一定是晶体
②NaCl晶体中与每个Na+距离相等且最近的Na+共有12个
③非极性分子中一定含有非极性键
④晶格能由大到小: NaF> NaCl> NaBr>NaI
⑤含有共价键的晶体一定具有高的熔、沸点及硬度
⑥s-s σ键与s-p σ键的电子云形状相同
⑦含有π键的化合物与只含σ键的化合物的化学性质不同
⑧中心原子采取sp3杂化的分子,其立体构形不一定是正四面体
| A.①②⑤⑥ | B.③④⑥⑦ | C.②④⑦⑧ | D.③④⑤⑧ |