有A、B、C、D四种金属片,进行如下实验:①A、B用导线相连后,同时浸入稀H2SO4溶液中,A极为负极;②C、D用导线连接后浸入稀H2SO4中,电流由D导线C;③A、C相连后同时浸入稀H2SO4中,C极产生大量气泡;④B、D相连后同时浸入稀H2SO4中,D极发生氧化反应,试判断四种金属的活动顺序是
A.A>B>C>D B.A>C>D>B C.C>A>B>D D.B>D>C>A
应用元素周期律,判断下列语句,其中正确的组合是()
①第三周期金属元素的最高价氧化物对应水化物,其碱性随原子序数的增大而减弱
②砹(At)是第VIIA族,其氢化物的稳定大于HC1
③硒(Se)与氧同主族,而与钙同周期,合成H2S比合成H2Se容易
④ 第二周期非金属元素的气态氢化物溶于水后,水溶液均为酸性
⑤铊(TI)与铝同主族,其单质既能与盐酸反应,又能与氢氧化钠溶液反应
| A.①③⑤ | B.①③ | C.①③④⑤ | D.全对 |
铝士矿的主要成分中含有氧化铝、氧化铁和二氧化硅等,工业上经过下列工艺可以冶炼金属铝。下列说法不正确的是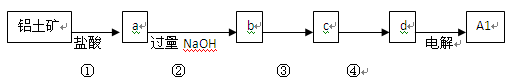
| A.①、②中除加试剂外。还需要进行过滤操作 |
| B.a 、b中铝元素的化合价相同 |
| C.③中需要通入过量的氨气 |
| D.④进行的操作是加热,而且d 一定是氧化铝 |
干燥剂的干燥性能值可用干燥效率(1 m3空气中实际残留水蒸气的质量)来衡量。某些干燥剂的干燥效率数据如下:
根据以上数据,下列叙述错误的是()
| A.上述干燥剂中阳离子对干燥效率的影响比阴离子小 |
| B.干燥效率可能与干燥剂的阴、阳离子的半径大小有关 |
| C.MgCl2可能是比CaCl2更好的干燥剂 |
| D.MgO的干燥性能比CaO好 |
等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间t产生氢气体积v的数据,根据数据绘制得到右下图,则曲线a所对应的实验组别是()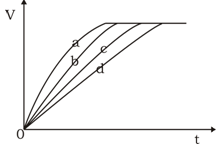
| 组别 |
c(HCl)(mol·L-1) |
温度(℃) |
状态 |
| A |
2.0 |
25 |
块状 |
| B |
2.5 |
30 |
块状 |
| C |
2.5 |
50 |
粉末状 |
| D |
2.5 |
50 |
块状 |
某含铬(Cr2O72-)废水用硫酸亚铁铵[FeSO4·(NH4)2SO4·6H2O]处理,反应后Cr和一部分Fe呈+3价,且反应后铁元素和铬元素完全转化为沉淀。该沉淀经干燥后得到n mol FeO·FeyCrxO3。不考虑处理过程中的实际损耗,下列叙述错误的是()
| A.消耗硫酸亚铁的物质的量为n(2-x) | B.处理废水中的Cr2O72-的物质的量为nx/2 |
| C.反应中发生转移的电子数为3nxmol | D.在FeO·FeyCrxO3中,3x="y" |