按下图所示装置进行实验,并回答下列问题:
(1)判断装置的名称:A池为 ,B池为 。
(2)锌极为 极,电极反应式为 ;铜极为 极,电极反应式为 ;石墨棒C1为 极,电极反应式为 ;石墨棒C2附近发生的实验现象为 ,反应结束后,B池溶液的pH值 。(增大、减小、不变,忽略气体溶于水) 。
(3)当C2极析出224 mL气体(标准状况下),锌的质量 (增加或减少) g。
W、X、Y、Z均为短周期主族元素,W的最外层电子数与核外电子总数之比为3∶8;X的核外电子总数与Y的最外层电子数相等,X的原子序数是Z的原子序数的一半;W、Y、Z位于同一周期。
(1)写出X的氢化物的电子式Z单质的晶体类型是类型
(2)W、Y、Z三种元素的气态氢化物稳定性由高到低的顺序是。(用化学式表示,Z的气态氢化物与其同主族元素气态氢化物化学式写法相似)。
(3)已知A、B、C、D四种物质存在如下反应关系:A+B―→C+D
①若A是Y和Z常见价态的化合物,B是X的氢化物,D是Y的氢化物,反应过程中没有化合价变化,该反应的化学方程式是。
②若A是Z的单质,B为红色固体,D为紫红色固体单质,高温下发生该反应,C的化学式是__________。D与X元素最高价氧化物对应水化物的浓溶液反应,生成的气体会对大气造成污染。用烧碱溶液吸收该气体生成两种盐,其中一种盐可用作防腐剂,烧碱溶液吸收气体的离子方程式是__________________。
某工业废水中仅含下表离子中的5种(不考虑水的电离及离子的水解),且各种离子的物质的量浓度相等,均为0.1mol/L。
| 阳离子 |
K+ Cu2+ Fe3+ Al3+ Fe2+ |
| 阴离子 |
Cl-CO32- NO3- SO42- SiO32- |
甲同学欲探究废水的组成,进行了如下实验:
Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察)。
Ⅱ.取少量溶液,加入KSCN溶液无明显变化。
Ⅲ.另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变。
Ⅳ.向Ⅲ中所得的溶液中加入BaCl2溶液,有白色沉淀生成。
请推断:(1)由Ⅰ、Ⅱ判断,溶液中一定不含有的阳离子是(写离子符号)。
(2)Ⅲ中加入少量盐酸生成无色气体的的离子方程式是_________________________。
(3)将Ⅲ中所得红棕色气体通入水中,气体变无色,所发生的化学方程式为:
(4)甲同学最终确定原溶液中所含阳离子是,阴离子是(写离子符号)。
(5)另取100mL原溶液,加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧至恒重,得到的固体质量为g。
直接排放含SO2的烟气会形成酸雨,危害环境。利用钠碱循环法可脱除烟气中的SO2.。
(1) 在钠碱循环法中,Na2SO3溶液作为吸收液,可由NaOH溶液吸收SO2制得,该反应的离子方程式是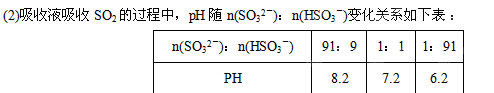
①由上表判断NaHSO3溶液显性,用化学平衡原理解释:
②当吸收液呈中性时,溶液中离子浓度关系正确的是(选填字母):
a.c(Na+) = 2c(SO32-)+c(HSO3-)
b.c(Na+)>c(HSO3-)>c(SO32-)>c(H+) = c(OH-)
c.c(Na+)+c(H+)=c(SO32-)+c(HSO3-)+c(OH-)
盐碱地(含较多NaCl、Na2CO3)不利于作物生长,通过施加适量石膏可以降低土壤的碱性。试用化学方程式分别表示盐碱地产生碱性的原因:,及用石膏降低其碱性的反应原理:。
请判断下列说法是否正确(填“对”或“错”)。
(1)碱性锌锰电池是一次电池,铅蓄电池是二次电池。
(2)随着温度的升高,纯水的pH增大。
(3)冰醋酸、纯碱、小苏打分别属于酸、碱、盐。
(4)镀锌铁制品破损后,镀层仍能保护铁制品。
(5)醋酸在醋酸钠溶液中电离的程度大于在纯水中电离的程度。
(6)25 ℃时,某物质的溶液pH<7,则该物质一定是酸或强酸弱碱盐。
(7)用Na2S去除废水中的Hg2+:Hg2++S2-=HgS↓
(8)pH=2与pH=1的硝酸中c(H+)之比为1:10
(9)Na2CO3溶液中c(Na+)与c(CO32-)之比为2:1
(10)向含有硫酸钙的水垢中加入碳酸钠溶液,沉淀的转化可表示为:
CaSO4(s)  SO42— + Ca2+
SO42— + Ca2+
CO32— CaCO3(s)
CaCO3(s)