W、X、Y、Z均为短周期主族元素,W的最外层电子数与核外电子总数之比为3∶8;X的核外电子总数与Y的最外层电子数相等,X的原子序数是Z的原子序数的一半;W、Y、Z位于同一周期。
(1)写出X的氢化物的电子式 Z单质的晶体类型是 类型
(2)W、Y、Z三种元素的气态氢化物稳定性由高到低的顺序是 。(用化学式表示,Z的气态氢化物与其同主族元素气态氢化物化学式写法相似)。
(3)已知A、B、C、D四种物质存在如下反应关系:A+B―→C+D
①若A是Y和Z常见价态的化合物,B是X的氢化物,D是Y的氢化物,反应过程中没有化合价变化,该反应的化学方程式是 。
②若A是Z的单质,B为红色固体,D为紫红色固体单质,高温下发生该反应,C的化学式是__________。D与X元素最高价氧化物对应水化物的浓溶液反应,生成的气体会对大气造成污染。用烧碱溶液吸收该气体生成两种盐,其中一种盐可用作防腐剂,烧碱溶液吸收气体的离子方程式是_______ ___________。
分子式为C2H6O的化合物A具有如下性质: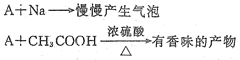
(1)根据上述信息,对该化合物可作出的判断是。
| A.一定含有—OH | B.一定含有—COOH |
| C.A为乙醇 | D.A为乙酸 |
(2)含A的体积分数为75%的水溶液可以用作。
(3)A与钠反应的化学方程式:。
(4)A可由含淀粉[(C6H10O5)n]的农产品如玉米、小麦、薯类等经发酵、蒸馏而得。请写出由淀粉制A的化学方程式:。
W、X、Y、Z是原子序数依次增大的同一短周期元素,W、X是金属元素,Y、Z是非金属元素。
(1)W、X各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式为。
(2)W与Y可形成化合物W2Y,该化合物的电子式为。
(3)Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为
。
(4)比较Y、Z气态氢化物的稳定性:>(用分子式表示)。
(5)W、X、Y、Z四种元素简单离子的离子半径由大到小的顺序是>>
>。
如下图所示,可形成氢氧燃料电池。通常氢氧燃料电池有酸式(当电解质溶液为硫酸时)和碱式[当电解质溶液为NaOH(aq)或KOH(aq)时]两种。试回答下列问题: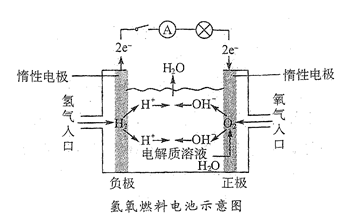
(1)酸式电池的电极反应:负极,正极;电池总反应:;电解质溶液pH的变化(填“变大”“变小”或“不变”)。
(2)碱式电池的电极反应:负极,正极;电池总反应:;电解质溶液pH的变化(填“变大”“变小”或“不变”)。
下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
| a |
|||||||||||||||||
| b |
c |
d |
e |
f |
|||||||||||||
| g |
h |
i |
j |
k |
l |
m |
|||||||||||
| n |
o |
||||||||||||||||

试回答下列问题:
(1)请写出元素O的基态原子电子排布式。
(2)第三周期8种元素按单质熔点高低的顺序如右图,其中序号“8”代表(填元素符号);其中电负性最大的是(填图中的序号)。
(3)由j原子跟c原子以1 : 1相互交替结合而形成的晶体,晶型与晶体j相同。两者相比熔点更高的是(填化学式),试从结构角度加以解释:
。
(4)i单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。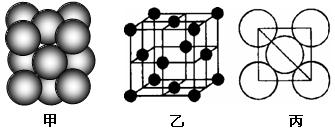
若已知i的原子半径为d,NA代表阿伏加德罗常数,i的相对原子质量为M,请回答:
①一个晶胞中i原子的数目为__;
②该晶体的密度为______(用字母表示)。
W、X、Y、Z四种元素的原子序数依次增大。其中Y原子的L电子层中,成对电子与未成对电子占据的轨道数相等,且无空轨道;X原子的L电子层中未成对电子数与Y相同,但还有空轨道;W、Z的原子序数相差10,且Z原子的第一电离能在同周期中最低。
(1)写出下列元素的元素符号:W,X,Y,Z。
(2)XY2分子中,X原子与Y原子都达到8电子稳定结构,则XY2分子中X和Y原子用于成键的电子数目分别是;根据电子云重叠方式的不同,分子里共价键的主要类型有。
(3)XY2与ZYW反应时,通过控制反应物的物质的量之比,可以得到不同的产物,相同条件下,在水中溶解度较小的产物是(写化学式),其原因是该化合物阴离子间可形成二聚离子或多聚链状离子。该化合物阴离子能够相互缔合的原因是: