(1)已知下列两个热化学方程式:
C3H8(g)+5O2(g) =3CO2(g)+4H2O(l) ΔH=-2220.0 kJ·mol-1
H2O(l)=H2O(g) ΔH="+44.0" kJ·mol-1
则0.5mol丙烷燃烧生成CO2和气态水时释放的热量为 。
(2)已知:TiO2(s)+2Cl2(g)=TiCl4(l)+O2(g) ΔH=+140 kJ·mol-1
2C(s)+O2(g)="2CO(g)" ΔH=-221 kJ·mol-1
写出TiO2和焦炭、氯气反应生成TiCl4和CO气体的热化学方程式: 。
(3)科学家已获得了极具理论研究意义的N4分子,其结构为正四面体(如图所示),与白磷分子相似。已知断裂1molN—N键吸收193kJ热量,断裂1molN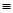 N键吸收941kJ热量,则1molN4气体转化为2molN2时要放出 kJ能量。
N键吸收941kJ热量,则1molN4气体转化为2molN2时要放出 kJ能量。
(4)阿波罗宇宙飞船上使用的是氢氧燃料电池,其电池总反应为:2H2+O2=2H2O,电解质溶液为稀H2SO4溶液,电池放电时是将 能转化为 能。其电极反应式分别为:负极 ,正极 。
(8分)参考下表中物质的熔点,回答有关有问题。
| 物质 |
NaF |
NaCl |
NaBr |
NaI |
NaCl |
KCl |
RbCl |
CsCl |
| 熔点/℃ |
995 |
801 |
755 |
651 |
801 |
776 |
715 |
646 |
| 物质 |
SiF4 |
SiCl4 |
SiBr4 |
SiI4 |
SiCl4 |
GeCl4 |
SnCl4 |
PbCl4 |
| 熔点/℃ |
-90.4 |
-70.4 |
5.2 |
120 |
-70.4 |
-49.5 |
-36.2 |
-15 |
(1)钠的卤化物及碱金属的氯化物的熔点与卤离子及碱金属离子的________________有关,随着________________的增大,熔点依次降低。
(2)硅的卤化物熔点及硅、锗、锡、铅的氯化物的熔点与________________________有关,随着________________增大,________________增大,故熔沸点依次升高。
(3)钠的卤化物的熔点比相应的硅的卤化物的熔点高得多,这与________________有关,因为一般________________比________________熔点高。
(14分)今有三种物质AC2、B2C2、AD4,元素A的最高正价和负化合价绝对值相等,元素B的单质能在C的气态单质中剧烈燃烧,火焰呈黄色,并生成淡黄色固体B2C2;
元素D的负一阶阴离子电子层结构与氩原子相同,则:
(1)A、B、C、D的元素符号为A_______________、B_______________、C_______________、D_______________。
(2)AC2、B2C2、AD4的电子式分别为_______________、______________、______________。
(3)AC2的分子空间构型是_______________,属于_______________ (填“极性”或“非极性”)分子。AD4分子的空间构型是______________,属于_____________(填“极性”或“非极性”)分子。
(4)B2C2中既含有_______________键,又含有_______________键,属于_______________ (填“离子”或“共价”)化合物。
(8分)含羟基的化合物可表示为M—OH(M不确定);当它与H+结合可后形成M—OH+
2离子(有机反应中的重要中间体);在一定条件下,易失去H+或H2O分子。请回答:
(1)符合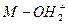 通式最简单的离子的电子式为____________________________________。
通式最简单的离子的电子式为____________________________________。
(2)粒子中原子数、电子数都相等的粒子称为等电子体。等电子体有相似的几何形状,上面(1)题中离子的几何形状为_____________________________。
(3)同温同压下,由A.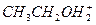 ;B.
;B.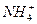 ;C.
;C. 三者分别形成的水溶液酸性由强到弱的顺序为____________________(填序号)。
三者分别形成的水溶液酸性由强到弱的顺序为____________________(填序号)。
(4)液态乙醇中存在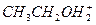 ,可与之相互中和而使液体呈中性的粒子为__________。
,可与之相互中和而使液体呈中性的粒子为__________。
a、b、c、d、e、f、g为七种由短周期元素构成的粒子,它们都有10个电子,其结构特
点如下:
粒子代码:a b c d e f g
原子核数:单核单核双核多核单核多核多核
电荷数: 0 1+ 1- 0 2+ 1+ 0
(单位电荷)
其中b的离子半径大于e的离子半径;d是由极性键构成的四原子极性分子;c与f可形成两
个共价型g分子。
试写出:(1)a粒子的原子结构示意图________________________________________.
(2)b与e相应元素的最高价氧化物对应水化物的碱性强弱比较为__________>__________(用化学式表示)。
(3)d溶于水的电离方程式__________________。
(4)g粒子所构成的晶体类型属__________________。
(5)c粒子是__________________,f粒子是__________________ (用化学式表示)。
氮可以形成多种离子,如: 等。已知
等。已知 的形成过程类似于
的形成过程类似于 的形成过程,
的形成过程, 在碱性溶液中生成电中性的分子和H2O,试填写下列空白:
在碱性溶液中生成电中性的分子和H2O,试填写下列空白:
(1)该电中性分子的化学式为 。
(2) 离子的电子式为 。
离子的电子式为 。
(3)一个 离子共有 个电子。
离子共有 个电子。
(4)写出两种由多原子组成的含有与 电子数相同的粒子的化学式: 。
电子数相同的粒子的化学式: 。