某研究小组以甲苯为主要原料,采用以下路线合成医药中间体F和Y。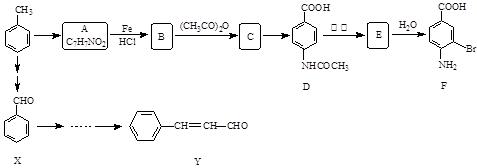
已知: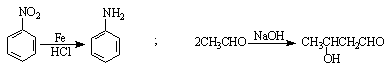
请回答下列问题:
(1)下列有关F的说法正确的是 。
| A.分子式是C7H7NO2Br | B.能形成内盐 |
| C.能发生取代反应和缩聚反应 | D.1 mol的 F最多可以和2 mol NaOH反应 |
(2)C→ D的反应类型是 。
(3)B→C的化学方程式是 。在合成F的过程中,B→C步骤不能省略,理由是 。
(4)写出同时符合下列条件的A的同分异构体的结构简式 。(要求写出3种)
①苯环上只有两种不同化学环境的氢原子;
②分子中含有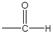 。
。
(5)以X和乙烯为原料可合成Y,请设计合成路线(无机试剂及溶剂任选)。
注:合成路线的书写格式参照如下示例流程图: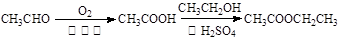
。
一项科学研究成果表明,铜锰氧化物(CuMn2O4)能在常温下催化氧化空气中的一氧化碳和甲醛(HCHO)。
(1)向一定物质的量浓度的Cu(NO3)2和Mn(NO3)2溶液中加入Na2CO3溶液,所得沉淀经高温灼烧,可制得CuMn2O4。
①Mn2+基态的电子排布式可表示为。
②NO3-的空间构型(用文字描述)。
(2)在铜锰氧化物的催化下,CO被氧化成CO2,HCHO被氧化成CO2和H2O。
①根据等电子原理,CO分子的结构式为。
②H2O分子中O原子轨道的杂化类型为。
(3)向CuSO4溶液中加入过量NaOH溶液可生成[Cu(OH)4]2-。不考虑空间构型,[Cu(OH)4]2-的结构可用示意图表示为。
将0.1molMg、Al混合物溶于100mL4mol/L的盐酸中,然后再滴加1mol/L的NaOH溶液,在滴加NaOH溶液的过程中,沉淀质量m与NaOH溶液的体积V的变化如图所示。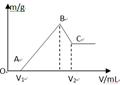
(1)写出BC过程的离子反应方程式
(2)当V1=140mL时,混合物中n(Mg)=_____mol,V2=_____mL
(3)滴入的NaOH溶液_____mL时,溶液中的Mg2+和Al3+刚好沉淀完全。
(4)若混合物中Mg的物质的量分数为a,当滴入的NaOH溶液为450mL时,所得沉淀中无Al(OH)3,则a的取值范围是____________________
(5)当加入V2 mlNaOH溶液后过滤,向滤液中通入过量的CO2气体,能观察到的现象为,写出该过程反应的离子方程式。
1.38g该有机物在纯氧中完全燃烧,可生成3.08g二氧化碳和0.54g水,同时消耗氧气2.24g。又知0.224L此有机物蒸气(已折算成标准状况下)的质量为1.38g。
⑴求此有机物的分子式。
⑵此有机物有多种同分异构体,且满足下列3个条件:
(i)遇FeCl3溶液显紫色
(ⅱ)能与NaHCO3溶液反应
(ⅲ)除苯环外无其它环状结构
请任意写出1种符合条件的此有机物的结构简式______________________;
⑶ 1mol此有机物分别与足量的碳酸氢钠溶液、氢氧化钠溶液反应理论上消耗二者的物质的量之比是。(要有计算过程)
某化工厂生产的某产品只含C、H、O三种元素,其分子模型如下图所示(图中球与球之间的连线代表化学键,如单键、双键等)。(1)该产品的结构简式为__________________________,
用1H核磁共振谱可以证明该化合物的核磁共振氢谱中有种吸收峰。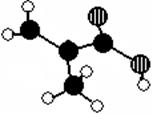
(2)下列物质中,与该产品互为同分异构体的是_____________(填序号),与该产品互为同系物的是_____________(填序号)。
①CH3CH=CHCOOH② CH2=CHCOOCH3③CH3CH2CH="CHCOOH" ④ CH3CH(CH3)COOH
(3)在一定条件下,该产品跟乙二醇反应可得到分子式为C6H10O3的物质,该物质发生加聚反应可得到用来制作隐形眼镜的高分子材料,请写出这种高聚物的结构简式:
____________________。
如图所示装置:
(1)若烧杯中溶液为稀硫酸,则观察到的现象为。
两极反应式为:正极;
负极,该装置将能转化为能。
(2)若烧杯中溶液为氢氧化钠溶液,则负极为,
总反应方程式为。