下列热化学方程式或离子方程式中,正确的是( )
| A.甲烷的标准燃烧热为-890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为: CH4(g)+2O2(g)===CO2(g)+2H2O(g)ΔH=-890.3 kJ·mol-1 |
B.500 ℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为:N2(g)+3H2(g)  2NH3(g) ; ΔH=-38.6 kJ·mol-1 2NH3(g) ; ΔH=-38.6 kJ·mol-1 |
| C.氯化镁溶液与氨水反应:Mg2++2OH-===Mg(OH)2↓ |
D.氧化铝溶于NaOH溶液:Al2O3+2OH-===2AlO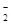 +H2O +H2O |
将2.32g Na2CO3、NaOH的固体混合物完全溶解于水,制成溶液,然后向该溶液中逐滴加入1 mol/L的盐酸,所加盐酸的体积与产生CO2的体积(标准状况)关系如下图所示,下列说法中错误的是
| A.OA段发生反应的离子方程式为:H++OH-===H2O CO32-+H+===HCO3- |
| B.当加入35mL盐酸时,产生CO2的体积为224mL |
| C.A点溶液中的溶质为NaC1、NaHCO3 |
| D.混合物中NaOH的质量0.60g |
向一定量的Cu、Fe2O3的混合物中加入100 mL 1 mol·L-1的盐酸,恰好使混合物完全溶解,所得溶液中不含Fe3+,若用过量的CO在高温下还原相同质量的原混合物,固体减少的质量为
| A.3.2 g | B.2.4 g | C.1.6 g | D.0.8 g |
甲、乙两种溶液中分别含有大量的Cu2+、K+、H+、Cl-、CO32-、OH-这6种离子中的3种(两种溶液中的离子不重复),已知甲溶液呈蓝色,则乙溶液中大量存在的离子是
| A.K+、OH-、CO32- | B.Cu2+、H+、Cl- |
| C.K+、H+、Cl- | D.CO32-、OH-、Cl- |
设NA代表阿伏加德罗常数,下列说法正确的是
| A.常温常压下,2克氢气所含原子数目为NA |
| B.4.6克钠与水反应时失去的电子数目为0.2NA |
| C.在标准状况下,22.4LNH3所含的质子数目为NA |
| D.1 L0.5mol•L-1Na2SO4溶液中所含有的Na+离子数目为2NA |
下列各组物质相互作用,生成物不随反应条件或反应物的用量变化而变化的是
| A.Na和O2 | B.FeCl3溶液和Mg |
| C.Fe和Cl2 | D.AlCl3溶液和NaOH |