碳和碳的化合物在生产、生活中的应用非常广泛,在提倡健康生活已成潮流的今天,“低碳生活”不再只是一种理想,更是一种值得期待的新的生活方式。
(1)甲烷燃烧放出大量的热,可作为能源用于人类的生产和生活。
已知:①2CH4(g)+3O2(g)=2CO(g)+4H2O(l) △H=" —1214" kJ/mol
②2CO(g)+O2(g)=2CO2(g) △H=" —566" kJ/mol
则表示甲烷燃烧热的热化学方程式 。
(2) 将两个石墨电极插入KOH溶液中,向两极分别通入CH4和O2,构成甲烷燃料电池。其负极电极反应式是: 。
(3)某同学利用甲烷燃料电池设计了一种电解法制取Fe(OH)2的实验装置(如下图所示),通电后,溶液中产生大量的白色沉淀,且较长时间不变色。下列说法中正确的是 (填序号)
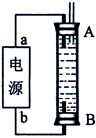
A.电源中的a一定为正极,b一定为负极
B.可以用NaCl溶液作为电解液
C.A、B两端都必须用铁作电极
D.阴极发生的反应是:2H+ + 2e-= H2↑
(4)将不同量的CO(g)和H2O(g)分别通入体积
为2L的恒容密闭容器中,进行反应:
CO(g)+H2O(g)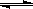 CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:
| 实验组 |
温度/℃ |
起始量/mol |
平衡量/mol |
达到平衡所需时间/min |
|
| H2O |
CO |
CO2 |
|||
| 1 |
650 |
2 |
4 |
1.6 |
5 |
| 2 |
900 |
1 |
2 |
0.4 |
3 |
| 3 |
900 |
1 |
2 |
0.4 |
1 |
①实验1中,以v (H2)表示的平均反应速率为 。
②实验3跟实验2相比,改变的条件可能是 (答一种情况即可)
在某澄清溶液中,可能存在下列几种离子:H+、K+、Ba2+、SO42-、I-、CO32-。取该溶液进行下列实验:①用pH试纸检验,该溶液呈强酸性;②取200mL溶液加入少量氯水和少量CCl4,振荡后静置,CCl4层呈紫色;③另取部分溶液逐滴加入NaOH溶液,当溶液呈碱性时,再加入Na2CO3溶液,有白色沉淀生成。
(1)根据上述实验现象,推断原溶液中肯定存在的离子是_____________,肯定不存在的离子是_______,可能存在的离子是____________。
(2)若步骤②中消耗0.1molCl2,则溶液中与Cl2反应的离子的物质的量浓度为________________。
(3)写出实验③中生成白色沉淀的离子方程式:__________________________。
明胶是水溶性蛋白质混合物,溶于水会形成胶体。工业明胶制成的胶囊中往往含有超标的重金属Cr,因而对人体造成伤害。
(1)用一束光照射明胶水溶液,可观察到_________现象。
(2)Na2CrO4是工业中常用的氧化剂,工业上可用FeCr2O4(Cr元素的化合价为+3)制Na2CrO4,其反应为4FeCr2O4+8Na2CO3+7O2==8Na2CrO4+2Fe2O3+8CO2。
①FeCr2O4中铁元素的化合价为_______,用氧化物的形式表示FeCr2O4的化学式:________。
②该反应的氧化产物是________;每生成1mol Na2CrO4时,转移电子_____mol。
已知Si与NaOH溶液反应的化学方程式为:Si+2NaOH+H2O=Na2SiO3+2H2↑。
(1)将等物质的量的下列物质投入到足量的烧碱溶液中,完全反应放出气体最多的是()
| A.硅 | B.铝 | C.钠 | D.铁 |
(2)将9.2 g钠和4.2 g硅同时投入到过量冷水中,充分反应后,在标准状况下,能生成氢气的体积是 L。
(1)AlCl3溶液与NaOH溶液反应时,当Al3+的物质的量与OH-的物质的量之比(以下均填物质的量之比)为________时,Al(OH)3沉淀量最多。
(2)NaAlO2溶液与盐酸溶液反应时,AlO的物质的量与H+的物质的量之比为________时,Al(OH)3沉淀恰好溶解。
将V mL NO和NO2的混合气体通过足量的水,充分反应后,得到一定体积的无色气体A。将此无色气体A与等体积的氧气混合,充分反应后,再通过足量的水,充分反应后还能收集到5 mL无色气体(以上气体体积均在相同状况下测定)。试回答:
(1)A是 ,其体积为 mL。
(2)反应过程中涉及的化学方程式: