制备氮化镁的装置示意图如下:

回答下列问题:
(1)检查装置气密性的方法是 ,
a的名称是 ,b的名称是 ;
(2)写出NaNO2和(NH4)2SO4反应制备氮气的化学方程式 ;
(3)C的作用是 ,D的作用是 ,是否可以把C和D的位置对调并说明理由 ;
(4)写出E中发生反应的化学方程式 ;
(5)请用化学方法确定是否有氮化镁生成,并检验是否含有未反应的镁,写出实验操作及现
象 。
Ⅰ.有甲、乙两位学生均想利用原电池反应检测金属的活动性顺序,两人均使用镁片和铝片作电极,但甲同学将电极放入2 mol/LH2SO4溶液中,乙同学将电极放入2 mol/L的NaOH溶液中,如图: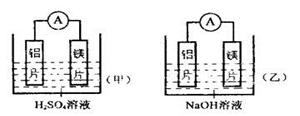
(1)写出甲池中正极的电极反应式:;
(2)写出乙池中负极的电极反应式:;
(3)如果甲与乙同学均认为“构成原电池的电极材料如果都是金属,则构成负极材料的金属应比构成正极材料的金属活泼”,则甲会判断出活动性更强,而乙会判断出活动性更强(填元素符号)。
(4)由此实验,可得到如下哪些正确结论?()
| A.利用原电池反应判断金属活动性顺序时应注意选择合适的电解质 |
| B.镁的金属性不一定比铝的金属性强 |
| C.该实验说明金属活动顺序表已过时,已设有实用价值 |
| D.该实验说明化学研究对象复杂、化学反应受条件影响较大,因此应具体问题具体分析 |
Ⅱ.向一个容积为2 L的密闭容器中充入2 mol A和1 mol B,发生如下反应:2 A(g) + B(g) 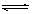 xC(g) + D(g),反应达到平衡时C的浓度为1.2 mol/L,B的浓度为0.1 mol/L。
xC(g) + D(g),反应达到平衡时C的浓度为1.2 mol/L,B的浓度为0.1 mol/L。
(1)x=;
(2)若使容器温度升高,平衡时混合气体的平均相对分子质量减小,则正反应为
(填“吸热”或“放热”)反应;
(3)若维持容器体积和温度不变,按下列方法加入起始物质,达到平衡时C的浓度仍为1.2 mol/L的是(用序号填空)
①4 mol A + 2 mol B
②3 mol C + 1 mol D
③3 mol C + 1 mol D +1 mol B
铁生锈是比较常见的现象,某实验小组,为研究铁生锈的条件,设计了以下快速.易行的方法: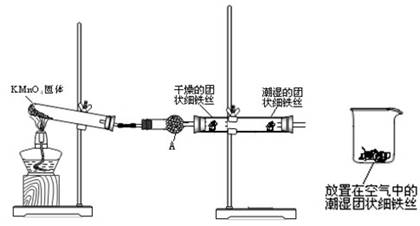

首先检查制氧气装置的气密性,然后按图连接好装置,点燃酒精灯给药品加热,持续3分钟左右,观察到的实验现象为:①直形管中用蒸馏水浸过的光亮铁丝表面颜色变得灰暗,发生锈蚀;②直形管中干燥的铁丝表面依然光亮,没有发生锈蚀;③中潮湿的铁丝依然光亮。
试回答以下问题:
(1)由于与接触的介质不同,金属腐蚀分成不同类型,本实验中铁生锈属于___________。
能表示其原理的反应方程式为_____________________________________
(2)仪器A的名称为______________,其中装的药品可以是_______________,其作用是___________________________________________
(3)由实验可知,该类铁生锈的条件为_______________________________________。决定铁生锈快慢的一个重要因素是_____________________________________________
下表是某城市某日的空气质量报告:
| 污染指数 |
首要污染物 |
空气质量级别 |
空气质量状况 |
| 55 |
SO2 |
II |
良 |
该市某校研究性学习小组对表中首要污染物SO2导致酸雨的成因进行了如下探究:
[探究实验一]用下图所示装置进行实验。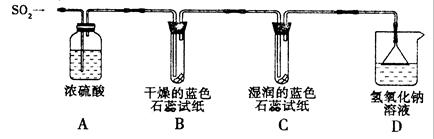
① A装置的作用是(填“干燥”或“氧化”)SO2气体。
②实验过程中,B装置内石蕊试纸的颜色没有发生变化,C装置内湿润的蓝色石蕊试纸变色,说明SO2与水反应生成一种酸。
③ D装置的作用是,D中发生反应的化学方程式是。
[探究实验二]往盛有水的烧杯中通入SO2气体,测得所得溶液的pH7(填“>”“=”或“<”),然后每隔1 h测定其pH,发现pH逐渐(填“变大”或“变小”),直至恒定。说明烧杯中的溶液被空气中的氧气氧化最终生成H2SO4。
[查阅资料]SO2形成酸雨的另一途径为:SO2与空气中的O2在飘尘的作用下反应生成SO3,SO3溶于降水生成H2SO4。则在此过程中的飘尘是作为(填“催化剂”或“氧化剂”)。
[探究结论]SO2与空气中的氧气、水反应生成硫酸而形成酸雨。该市可能易出现酸雨。
[知识拓展]
(1)汽车排放的尾气,硝酸、化肥等工业生产排出的废气中都含有氮的氧化物,氮的氧化物溶于水最终转化为,是造成酸雨的另一主要原因。
(2)该市某工厂的燃料煤中硫的质量分数为0.16%,该工厂每天燃烧这种煤100吨。如果煤中的硫全部转化为SO2,那么这些SO2在标准状况下的体积约为m3。
某化学兴趣小组在探究次氯酸钠溶液的性质时发现:
往过量FeSO4溶液中滴入几滴NaClO溶液,并加入适量硫酸,溶液立即变黄。
请你协助他们完成该反应还原产物的探究。
(1)甲同学推测该反应的还原产物为Cl2;乙同学推测该反应的还原产物为。
(2)假设乙同学的推测是正确。
写出过量FeSO4溶液中,滴入几滴NaClO溶液,并加入适量硫酸的离子方程式:
。
请你设计一个实验方案,验证乙同学的推测是正确的。
要求在答题卡上按下表格式写出实验步骤、预期现象和结论(可以不填满):
| 实验操作 |
预期现象和结论 |
| 步骤1:取上述反应后的溶液少许于试管A中, 。 |
|
| 步骤2: 。 |
|
| 步骤3: 。 |
(1)浓硫酸和木炭(C)加热时反应的化学方程式为:
;
为了验证反应的全部生成物,用下图装置进行实验。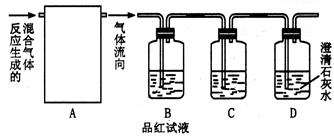
(2)上图A处是完成实验的必要装置,它是下列图中的(填编号);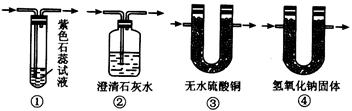
(3) C装置中盛放的试剂为,
其作用是;
(4)能够证明存在CO2气体的实验现象是:
。