【化学——物质结构与性质】金属镍在电池、合金、催化剂等方面应用广泛。
(1)下列关于金属及金属键的说法正确的是_______。
a.金属键具有方向性和饱和性
b.金属键是金属阳离子与自由电子间的相互作用
c.金属导电是因为在外加电场作用下产生自由电子
d.金属具有光泽是因为金属阳离子吸收并放出可见光
(2)Ni是元素周期表中第28号元素,第二周期基态原子未成对电子数与Ni相同且电负性最小的元素是______。
(3)过渡金属配合物Ni(CO)的中心原子价电子数与配体提供电子总数之和为18,则n=______。CO与N2结构相似,CO分子内o- 建于π键个数之比为________。
(4)甲醛(H2C=O)在Ni催化作用下加氢可得甲醛(CH2OH)。甲醛分子内C原子的杂化方式为________,甲醛分子内的O—C—H键角_______(填“大于”“等于”或“小于”)甲醛分子内的O—C—H键角。
形成油脂的脂肪酸的饱和程度对油脂的熔点有着重要的影响,由________的脂肪酸生成的甘油酯熔点较高,常温下呈________态;由的脂肪酸生成的甘油酯熔点较低,常温下呈________态。
葡萄糖结构简式为 ,官能团名称为和
,官能团名称为和 ,能发生银镜反应,化学方程式是。淀粉分子式为,遇碘水变成________色,有些蛋白质遇浓硝酸变成________色。
,能发生银镜反应,化学方程式是。淀粉分子式为,遇碘水变成________色,有些蛋白质遇浓硝酸变成________色。
某研究小组在实验室探究氨基甲酸铵(NH2COONH4)分解反应平衡常数和水解反应速率的测定。
(1)将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s) 2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表:
2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表:
| 温度(℃) |
15.0 |
20.0 |
25.0 |
30.0 |
35.0 |
| 平衡总压强(kPa) |
5.7 |
8.3 |
12.0 |
17.1 |
24.0 |
| 平衡气体总浓度(×10-3mol/L) |
2.4 |
3.4 |
4.8 |
6.8 |
9.4 |
①可以判断该分解反应已经达到化学平衡的是___________。
A.2v(NH3)= v(CO2)B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变D.密闭容器中氨气的体积分数不变
②根据表中数据,列式计算25.0℃时的分解平衡常数:K=_____=。
③取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25℃下达到分解平衡。若在恒温下压缩容器体积,氨基甲酸铵固体的质量______(填“增加”、“减小”或“不变”)。
④氨基甲酸铵分解反应的焓变△H____0,熵变△S___0(填>、<或=)。
(2)已知:NH2COONH4+2H2O NH4HCO3+NH3·H2O。该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定水解反应速率,得到c(NH2COO-)随时间变化趋势如图所示。
NH4HCO3+NH3·H2O。该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定水解反应速率,得到c(NH2COO-)随时间变化趋势如图所示。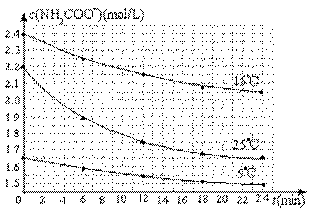
⑤计算25℃时,0~6min氨基甲酸铵水解反应的平均速率______________。
⑥根据图中信息,如何说明水解反应速率随温度升高而增大:___________。
常温下,某水溶液M中存在的离子有:Na+、A2-、HA-、H+、OH-,存在的分子有H2O、H2A。根据题 意回答下列问题:
意回答下列问题:
(1)写出酸H2A的电离方程式。
(2)若溶液M由10 mL 2 mol·L-1NaHA溶液与2 mol·L-1NaOH溶液等体积混合而得,则溶液M的pH________7(填“>”、“<”或“=”),溶液中离子浓度由大到小顺序为。
(3)若溶液M由下列三种情况:①0.01 mol·L-1的H2A溶液;②0.01 mol·L-1的NaHA溶液;③0.02 mol·L-1的HCl与0.04 mol·L-1的NaHA溶液等体积混合液,则三种情况的溶液中H2A分子浓度最大的为________;pH由大到小的顺序为____________。
(4)若溶液M由pH=3的H2A溶液V1 mL与pH=11的NaOH溶液V2 mL混合反应而得,混合溶液c(H+)/c(OH-)=104,V1与V2的大小关系为__________(填“大于”“等于”“小于”或“均有可能”)。
将等物质的量的A、B、C、D四种物质混合,发生如下反应:aA+bB cC(s)+dD,当反应进行一定时间
cC(s)+dD,当反应进行一定时间 后,测得A减少了nmol,B减少了1/2 n mol,C增加了3/2 n mol,D增加了n mol,此时达到化学平衡。请填写下列空白:
后,测得A减少了nmol,B减少了1/2 n mol,C增加了3/2 n mol,D增加了n mol,此时达到化学平衡。请填写下列空白:
(1)该化学方程式各物质的化学计量数为a=_____、b=______、c=_____、d=______。
(2)若只改变压强,反应速率发生变化,但平衡不发生移动,该反应中物质D的聚集状态为______。
(3)若只升高温度, 反应一段时间后,测知四种物质其物质的量又达到相等,则该反应为________反应(填“放热”或“吸热”)。
反应一段时间后,测知四种物质其物质的量又达到相等,则该反应为________反应(填“放热”或“吸热”)。