某研究小组在实验室探究氨基甲酸铵(NH2COONH4)分解反应平衡常数和水解反应速率的测定。
(1)将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s) 2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表:
2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表:
| 温度(℃) |
15.0 |
20.0 |
25.0 |
30.0 |
35.0 |
| 平衡总压强(kPa) |
5.7 |
8.3 |
12.0 |
17.1 |
24.0 |
| 平衡气体总浓度(×10-3mol/L) |
2.4 |
3.4 |
4.8 |
6.8 |
9.4 |
①可以判断该分解反应已经达到化学平衡的是___________。
A.2v(NH3) = v(CO2) B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变 D.密闭容器中氨气的体积分数不变
②根据表中数据,列式计算25.0℃时的分解平衡常数:K=_____= 。
③取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25℃下达到分解平衡。若在恒温下压缩容器体积,氨基甲酸铵固体的质量______(填“增加”、“减小”或“不变”)。
④氨基甲酸铵分解反应的焓变△H____0,熵变△S___0(填>、<或=)。
(2)已知:NH2COONH4+2H2O NH4HCO3+NH3·H2O。该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定水解反应速率,得到c(NH2COO-)随时间变化趋势如图所示。
NH4HCO3+NH3·H2O。该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定水解反应速率,得到c(NH2COO-)随时间变化趋势如图所示。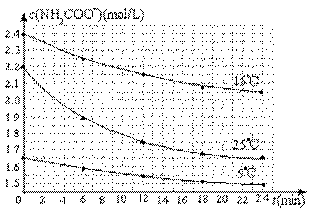
⑤计算25℃时,0~6min氨基甲酸铵水解反应的平均速率______________。
⑥根据图中信息,如何说明水解反应速率随温度升高而增大:___________。
将FeSO4·a(NH4)2SO4·bH2O的晶体9.6g与过量的氯化钡溶液反应,生成11.417gBaSO4;然后加入足量浓NaOH溶液并加热,产生的氨气用100ml 1mol/L盐酸吸收,剩余的盐酸再用2mol/LNaOH溶液中和,需NaOH溶液25.5ml。则
(1)9.6g晶体中SO42—离子的物质的量是_________________________
(2)晶体化学式中a、b的值是(均取整数):a=________;b=____________
(12分)(2004江苏高考题)下图中,A是一种无色液体,G是极易溶于水的碱性气体,Y是胃酸的主要成分,K是不溶于稀硝酸的白色沉淀,反应⑤是工业制X的主要反应之一。
请按要求填空:
(1)写出下列物质的化学式:A:,E:
F:,Y:。
(2)反应⑤的化学方程式为:。
(3)1molB通过反应②得到1molF,B中F的质量分数为72%,则B的化学式为:。
(8分)微生物对人类有着各种各样的用途,现在生物工程学家利用微生物从矿石中提取金属。铜是一种很有价值的金属,可以从铜矿中提取。微生物法是采用某些细菌能用空气中的氧气氧化硫化铜矿石,把不溶性的硫化铜转化成可溶的硫酸铜。利用细菌提取铜的生产过程:在已有细菌存在的岩石、矿石堆中,喷洒酸水以促进细菌生长;在它们的生长过程中,氧化而成的硫酸铜形成低浓度的溶液流到矿石堆的底部,再从这种溶液中提取金属铜。水循环使用,再回到矿石堆中。在美国,10%的铜是用这种方法生产的。
试回答下列问题:
(1)细菌把硫化铜氧化为硫酸铜的过程中起了什么作用:
(2)从硫酸铜溶液中提取铜,简便而经济的方法是;相应的化学方程式为:
(3)普通生产铜的方法是在空气中燃烧硫化铜(产物中有一种气态氧化物)。试比较两种方法的优缺点。
(10分)(1)用地壳中某主要元素生产的多种产品在现代高科技中占重要位置,足见化学对现代物质文明的重要作用。例如:
①光导纤维的主要成分是;
②目前应用最多的太阳能电池的光电转化材料是。
(2)氮化硅Si3N4是一种高温结构材料,粉末状态的Si3N4可以由SiCl4的蒸气和NH3反应制取。粉末状Si3N4对空气和水都不稳定。但将粉末状的Si3N4和适量氧化镁在230×1.01×105Pa和185℃的密闭容器中热处理,可以制得结构十分紧密、对空气和水都相当稳定的固体材料,同时还得到对水不稳定的Mg3N2。
①写出由SiCl4和NH3反应制取Si3N4的化学反应方程式:;
②在Si3N4和适量氧化镁在230×1.01×105Pa和185℃的密闭容器中热处理的过程中,发生反应,反应过程中有Mg3N2生成。其化学方程式为:;
③氮化硅Si3N4是一种高温结构材料,其优点是(只要求写出二种)。
、
(8分)某工厂排出的废水中含氯气,为了除去废水中游离态氯,而且使废水变为中性,有人提出如图所示方案。在废水排出管的A、B处分别注入一定流量的废烧碱溶液和亚硫酸钠溶液。
试写出:(1)A、B处应加入的物质的化学式为______________,_______________。
(2)A、B处反应离子方程式:
A:_________________________。B:_________________。