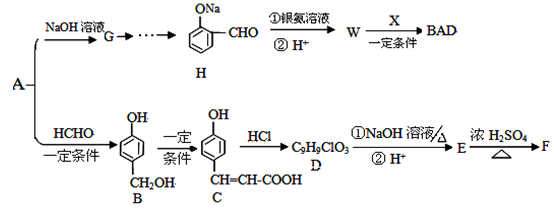
中学化学常见有机物A(C6H6O)能合成紫外线吸收剂BAD和某药物中间体F,合成路线为:
已知:BAD的结构简式为:、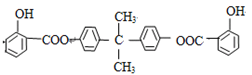
F的结构简式为: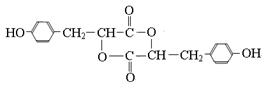
C中含氧官能团的名称 ,W的结构简式 。
(2)反应类型 A→B 。
(3)1mol C充分反应可以消耗 mol Br2 ;C和过量 NaOH溶液反应的化学方程式 。
(4)C→D的过程中可能有另一种产物D1,D1的结构简式 。
(5)E的结构简式为 。反应类型 E→F 。
(6)W的同分异构体有多种,写出一种符合以下要求的W的同分异构体的结构简式:
① 遇FeCl3溶液呈紫色; ② 能发生银镜反应;③ 苯环上的一氯代物只有两种。 。
已知氨气的化学式是NH3,其相对分子质量为_________,其摩尔质量为_________;6.8g NH3的物质的量为__________mol,其标准状况下的体积为__________L,其含NH3分子的个数为_______,含有氢原子的
个数为___________ 。
铁丝在氯气中点燃发生反应:2Fe + 3Cl2  2FeCl3,其中氯元素的化合价_______(填“升高”或“降低”),氯元素被_________(填“氧化”或“还原”);Fe做_________剂,具有性。在该反应中,若消耗了1 mol Fe,则生成_______mol FeCl3,转移mol电子。
2FeCl3,其中氯元素的化合价_______(填“升高”或“降低”),氯元素被_________(填“氧化”或“还原”);Fe做_________剂,具有性。在该反应中,若消耗了1 mol Fe,则生成_______mol FeCl3,转移mol电子。
对无机化合物可根据其组成和性质进行如下分类: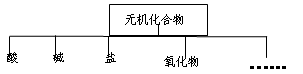
(1)上图所示的物质分类方法可称为。
(2)以Na、H、C、N、O、S、Cl等元素中任选两种或三种元素组成合适的一种物质,将其化学式分别填在下表中的相应位置。
| 物质 类别 |
酸 |
碱 |
盐 |
氧化物 |
| 化学式 |
用18.4mol/L的浓H2SO4配制100mL 0.50mol/L的稀H2SO4,请按要求填空(每空 1分,共计 10分)
(1)用量筒量取所需浓H2SO4的体积为mL;
(2)如果实验室有10mL、20mL、50mL量筒,应选用mL量筒,实验中还需要用到的仪器有、 、烧杯、玻璃棒。
(3)若实验中出现下列现象对所配溶液浓度有什么影响?(填偏高、偏低、无影响)
①浓硫酸溶解后未冷至室温即进行定容
②定容时俯视刻度线
③容量瓶洗净后未干燥;
④摇匀后发现液面低于刻度线后加水至溶液的凹液面与刻度线相平;
⑤用量筒量取浓H2SO4时仰视刻度线:。
(4)若定容时液面高于刻度线应采取的措施是。
某工厂在山坡坑道的仓库里贮有氯气钢瓶。某天,有一只贮有氯气的钢瓶损坏,造成氯气泄漏,在场工人采取以下措施,请选择填充并简述理由。(每空1分,共计5分)
(1)处理钢瓶的方法正确的是,
A、钢瓶推到坡下的小河里
B、把钢瓶丢到深坑里,用熟石灰填埋
C、把钢瓶扔到农田中;
简述理由
(2)钢瓶处理后,工人应立即,
A、转移到坡下 B、转移到坡上
简述理由
(3)若在场工人没有防毒面具,可以用浸有某种物质的一定浓度的水溶液的毛巾捂住鼻子,最适宜采用的物质是。
A、NaOH B、NaClC、Ca (OH)2D、Na2CO3