肉桂醛在食品、医药化工等方面都有应用。
(1)质谱分析肉桂醛分子的相对分子质量为132。其分子中碳元素的质量分数为82%,其余为氢和氧。分子中的碳原子数等于氢、氧原子数之和。肉桂醛的分子式是 。
(2) 肉桂醛具有下列性质:
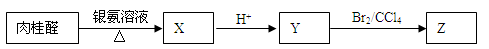
请回答:
① 肉桂醛是苯的一取代物,核磁共振氢谱显示,苯环侧链上有三种不同化学环境的氢原子,其结构简式是 。(本题均不考虑顺反异构与手性异构)
② Z不能发生的反应类型是 。
| A.取代反应 | B.消去反应 | C.加成反应 | D.加聚反应 |
③ Y与乙醇在一定条件下作用得到肉桂酸乙酯,该反应的化学方程式是 。
④ Y的同分异构体中,属于酯类且苯环上只有一个取代基的同分异构体有 种,其中任意一种的结构简式是 。
(3)已知
Ⅰ、醛与醛能发生反应,原理如下:
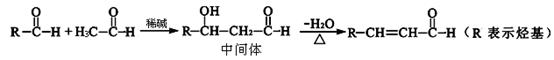
Ⅱ、合成肉桂醛的工业流程如下图所示(甲为烃):
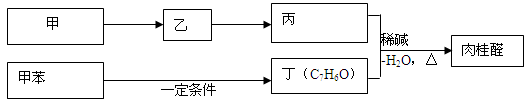
请回答:
①甲的结构简式是 。
②写出丙和丁生成肉桂醛的化学方程式是 。
已知R—CH==CH2+HX (主要产物)。下图中的A、B分别是分子式为C3H7Cl的两种同分异构体,请根据图中所示物质转化关系和反应条件,判断并写出:
(主要产物)。下图中的A、B分别是分子式为C3H7Cl的两种同分异构体,请根据图中所示物质转化关系和反应条件,判断并写出: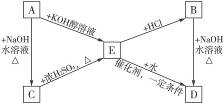
(1)A、B、C、D、E的结构简式。
(2)由E转化为B,由D转化为E的化学方程式。
能发生消去反应,生成物中存在同分异构体的是()
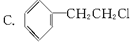
D.CH3Cl
有液态卤代烃C7H7X,为测定分子中卤原子的种类和卤代烃的分子结构,设计了如下实验步骤。
①取卤代烃适量与过量稀NaOH溶液放于锥形瓶中混合,塞上带长玻璃管的瓶塞,加热、充分反应②将反应后的液体分成两份,分装在两支试管中③在一支试管中滴加AgNO3溶液,观察沉淀的颜色以确定卤原子种类④在另一支试管中滴加溴水、无明显变化
回答:
(1)装置中长玻璃管的作用是__________________。
(2)步骤③能否确定卤原子的种类?____________________(填“能”或“不能”),理由是___________________________________________________。
(3)若步骤③最终观察到产生淡黄色沉淀,则该卤代烃的结构简式是_________________,水解产物的名称是_____________________________,判断的理由是_____________________。
从CH3CH2CH2Cl、Cl2、HNO3、NaOH、乙醇、H2O中选用必要的原料,经最佳途径合成CH2ClCHClCH3,写出有关反应的化学方程式。
写出分子组成为C5H11Br的有机物的同分异构体中,只能发生水解反应,不能发生消去反应的物质的结构简式,并命名。