相同温度下,在体积相等的三个恒容密闭容器中发生可逆反应:N2(g)+3H2(g)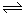 2NH3(g)△H=-92.4kJ/mol,实验测得起始、平衡时的有关数据如下表:
2NH3(g)△H=-92.4kJ/mol,实验测得起始、平衡时的有关数据如下表: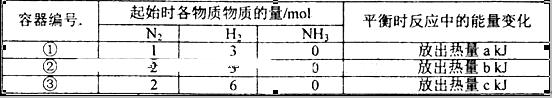
下列叙述正确的是
| A.放出热量关系:a<b <92.4 |
| B.三个容器内反应的平衡常数:③>①>② |
| C.达平衡时氨气的体积分数:①>③ |
| D.N2的转化率:②>①>③ |
NA表示阿伏伽德罗常数的数值,下列说法正确的是
| A.标准状况下22.4L任意比的氢气和二氧化碳的混合气体中含有的分子总数均为NA |
| B.0.1mol/LNaCl溶液中Na+的数目为0.1NA |
| C.标准状况下,5.6L四氯化碳含有的分子数为0.25NA |
| D.500mL0.2mol/L饱和FeCl3溶液完全转化可制得0.1NA个Fe(OH)3胶粒 |
向存在大量Na+、Cl-的溶液中通入足量的NH3后,该溶液中还可能大量存在的离子组是
| A.K+、Br-、CO32- | B.Al3+、H+、MnO4- | C.NH4+、Fe3+、SO42- | D.Ag+、Cu2+、NO3- |
臭氧可以使湿润的淀粉碘化钾试纸变蓝,化学方程式为:KI+O3+H2O→KOH+I2+O2(未配平)下列叙述正确的是
| A.O3在反应中被还原为O2 |
| B.1molO3在反应中得到2mol电子 |
| C.该反应的还原产物为I2 |
| D.反应中氧化产物与还原产物物质的量之比为1:3 |
2.3g纯净物金属钠在干燥空气中被氧化后得到3.5g固体,由此判断其氧化产物为
| A.Na2O | B.Na2O2 | C.Na2O和Na2O2 | D.无法确定 |
下列离子检验的方法正确的是
| A.某溶液中滴加AgNO3溶液有白色沉淀,说明原溶液中有Cl- |
| B.某溶液中先滴加足量盐酸无规象,再滴加BaCl2溶液有白色沉淀.则原溶液中有SO42- |
| C.某无色溶液滴入酚酞试液显红色,该溶液一定是含有大量的H+ |
| D.某溶液中滴加盐酸生成能使澄清石灰水变浑浊的无色气体,说明原溶液中有CO32- |