短周期元素X、Y、Z、W的原子序数依次增大,X 原子的最外层电子数是其内层电子总数的3 倍,Y 原子的最外层只有2 个电子,Z 单质可制成半导体材料,W与X属于同一主族。下列叙述正确的是
| A.元素W 的简单气态氢化物的热稳定性比X 的强 |
| B.元素W 的最高价氧化物对应水化物的酸性比Z 的弱 |
| C.化合物YX、ZX2、WX3中化学键的类型相同 |
| D.原子半径的大小顺序: r(Y)>r(Z)>r(W) >r(X) |
使用含铅汽油能使空气中的铅含量增多,引起铅中毒。下列说法中,正确的是()
| A.铅笔芯的主要成分是金属铅 |
| B.CO气体有毒,在生有炉火的居室中多放几盆水,可吸收CO |
| C.臭氧层的破坏对人类健康有害 |
| D.绿色食品是指使用过化肥和农药生产出来的农副产品 |
将镁片、铝片平行插入到一定浓度的NaOH溶液中,用导线连接成闭合回路,该装置在工作时,下列叙述正确的是
| A.镁比铝活泼,镁失去电子被氧化成Mg2+ |
| B.铝是电池负极,开始工作时溶液中会立即有白色沉淀生成 |
| C.该装置的内、外电路中,均是电子的定向移动形成电流 |
| D.该装置开始工作时,铝片表面的氧化膜可不必处理 |
下列有关溶液的叙述正确的是
| A.常温下的醋酸铵溶液呈中性,则溶液中c(H+)=c(OH-)=10-7mol·L-1 |
| B.在pH=2的醋酸溶液中加入等体积c(酸)=2mol·L-1的某酸溶液后,混合溶液的pH一定会减小 |
| C.pH相同的醋酸溶液和盐酸,分别用蒸馏水稀释至原溶液的m倍和n倍,若稀释后两溶液的pH仍相同,则m>n |
| D.导电性强的溶液中自由移动离子数目一定比导电性弱的溶液中自由移动离子数目多 |
25℃时,在25mL0.1mol/L的氢氧化钠溶液中,逐滴加入0.2mol/LCH3COOH,溶液的pH的变化曲线如图所示,下列分析的结论正确的是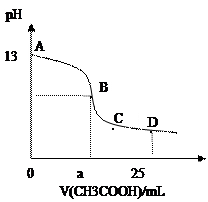
A.B点的横座标a==12.5,且有c(Na+)==c(CH3COO—)
B.C点时,c(CH3COO—)>c(Na+)>c(H+)= c(OH—)
C.D点时,c(CH3COO—)+ c(CH3COOH)==2c(Na+)
D.对曲线上A、B间任何一点,溶液中都有:
c(Na+)>c(CH3COO—)>c(OH—) >c(H+)
在容积固定的密闭容器中存在如下反应:A(g)+3B(g) 2C(g);△H<0
某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出下列关系图: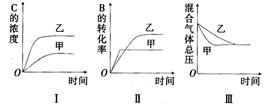
下列判断一定错误的是
| A.图I研究的是不同催化剂对反应的影响,且乙使用的催化剂效率较高 |
| B.图Ⅱ研究的是压强对反应的影响,且甲的压强较高 |
| C.图Ⅱ研究的是温度对反应的影响,且甲的温度较高 |
| D.图Ⅲ研究的是不同催化剂对反应的影响,且甲使用的催化剂效率较高 |