从能量的变化和反应的快慢等角度研究反应: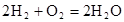 。
。
(1)为了加快正反应速率,可以采取的措施有________(填序号,下同)。
| A.使用催化剂 | B.提高氧气的浓度 |
| C.提高反应的温度 | D.降低反应的温度 |
(2)已知该反应为放热反应,下图能正确表示该反应中能量变化的是________。
(3)从断键和成键的角度分析上述反应中能量的变化。已知:化学键的键能:
| 化学键 |
H—H |
O=O |
H—O |
键能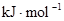 |
436 |
496 |
463 |
由此计算2molH2在氧气中燃烧生成气态水放出的热量
(4)已知1克氢气完全燃烧生成液态水放出QKJ的热量,则氢气燃烧生成液态水的热化学反应方程式为
(5)氢氧燃料电池的总反应方程式为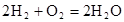 。其中,氢气在________(填“正”或“负”)极发生________反应(填“氧化”或“还原”)。电路中每转移0.2mol电子,标准状况下消耗H2的体积是________L。
。其中,氢气在________(填“正”或“负”)极发生________反应(填“氧化”或“还原”)。电路中每转移0.2mol电子,标准状况下消耗H2的体积是________L。
.(本题16分)已知醛或酮可以发生如下反应: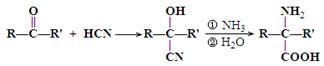
苯丙氨酸( )是合成APM的原料之一。APM的结构简式如图所示。
)是合成APM的原料之一。APM的结构简式如图所示。
(1)指出APM的结构中含氧官能团的名称__________
(2)下列关于APM的说法中,正确的是 _。
A属于糖类化合物 B分子式为C14H18N2O5
C既能与酸反应,又能与碱反应
D能发生酯化反应,但不能发生加成反应
E1 molAPM与NaOH反应最终生成1mol H2O
(3)APM在酸性环境水解的产物中,相对分子质量为133的有机物与氨基乙酸(H2N-CH2COOH)以1:1发生缩合反应形成一个含有六元环的化合物。该环状化合物的结构简式为。
(4)苯丙氨酸的一种合成途径如下图所示: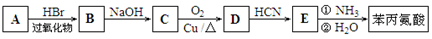
①烃 A的结构简式为。1 molD完全燃烧消耗O2_______mol.
② 写出C → D反应的化学方程式:.
③ 某苯的同系物苯环上的一硝基取代物只有一种,该硝基取代物W是苯丙氨酸的同分异构体。W的结构简式为。
工业上设计将VOSO4中的K2SO4、SiO2杂质除去并回收得到V2O5的流程如下:
请回答下列问题:
(1)步骤①所得废渣的成分是(写化学式),操作I的名称。
(2)步骤②、③的变化过程可简化为(下式R表示VO2+,HA表示有机萃取剂):
R2(SO4)n (水层)+ 2nHA(有机层) 2RAn(有机层) + nH2SO4 (水层)
2RAn(有机层) + nH2SO4 (水层)
②中萃取时必须加入适量碱,其原因是。
③中X试剂为 。
(3)④的离子方程式为。
(4)25℃时,取样进行试验分析,得到钒沉淀率和溶液pH之间关系如下表:
| pH |
1.3 |
1.4 |
1.5 |
1.6 |
1.7 |
1.8 |
1.9 |
2.0 |
2.1 |
| 钒沉淀率% |
88.1 |
94.8 |
96.5 |
98.0 |
98.8 |
98.8 |
96.4 |
93.1 |
89.3 |
结合上表,在实际生产中,⑤中加入氨水,调节溶液的最佳pH为;若钒沉淀率为93.1%时不产生Fe(OH)3沉淀,则溶液中c(Fe3+)<。〖已知:25℃时,Ksp[Fe(OH)3]=2.6×10-39〗
(5)该工艺流程中,可以循环利用的物质有和。
(13分)平板电视显示屏生产过程中产生大量的废玻璃粉末(含SiO2、Fe2O3、CeO2、FeO等物质)。某课题以此粉末为原料,设计如下工艺流程对资源进行回收,得到Ce(OH)4和硫酸铁铵:
已知:
ⅰ.酸性条件下,铈在水溶液中有 、
、 两种主要存在形式,
两种主要存在形式, 易水解,
易水解, 有较强氧化性。
有较强氧化性。
ⅱ.CeO2不溶于稀硫酸
ⅲ.硫酸铁铵[aFe2(SO4) 3·b(NH4) 2SO4·cH2O]广泛用于水的净化处理。
(1).操作Ⅰ的名称是 ,检验硫酸铁铵溶液中含有NH4+的方法是: 。
(2).反应①之前先要洗涤滤渣B,其目的是为了除去 (填离子符号)。
(3).写出反应①的化学方程式 。
(4).用滴定法测定制得的Ce(OH)4产品纯度。
滴定时所用定量仪器的读数精确为 ;若所用FeSO4溶液在空气中露置一段时间后再进进行滴定,则测得该Ce(OH)4产品的质量分数 。(填“偏大”、“偏小”或“无影响”)
(5).称取14.00g硫酸铁铵样品,将其溶于水配制成100mL溶液,分成两等份,向其中一份加入足量NaOH溶液,过滤洗涤沉淀并烘干灼烧至恒重得到1.60g固体;向另一份溶液中加入0.5mol/L Ba(NO3)2溶液100mL,恰好完全反应。则该硫酸铁铵的化学式为 。
【化学选修5——有机化学基础】
姜黄素(分子式为C21H20O6)存在姜科植物姜黄等的根茎中,具有抗基因突变和预防肿瘤的作用。其合成路线如下: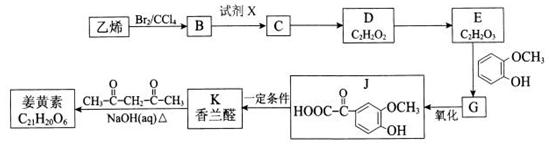
已知:
i.
ii.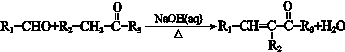
(R1、R2、R3为烃基或氢原子)
iii. E的核磁共振氢谱中有两个峰
请回答下列问题:
(1)E中含有的官能团名称是。
(2)B物质的名称为;试剂X为。
(3)姜黄素的结构简式为。
(4)E →G反应的化学方程式为;其反应类型是 。
(5)下列有关香兰醛的叙述正确的是(填正确答案编号)。
a.香兰醛能与NaHCO3溶液反应
b.香兰醛能与浓溴水发生取代反应
c.能与FeCl3溶液发生显色反应
d.1 mol香兰醛最多能与3 molH2发生加成反应
(6)符合下列条件的香兰醛(K)的同分异构体有种:①属于芳香族化合物 ②与氯化铁溶液发生显色反应 ③苯环上只有两个取代基 ④存在羰基的结构。写出香兰醛(K)的同分异构体中符合下列条件的结构简式。
①苯环上的一氯取代物只有2种;
②1mol该物质与烧碱溶液反应,最多消耗3molNaOH;
③核磁共振氢谱中有4种吸收峰。
乙醇、乙酸都是有机化工重要的基础原料。
(1).空气中,乙醇蒸气能使红热铜丝保持红热,该反应的化学方程式为。
(2).浓硫酸催化下,乙酸和乙醇生成乙酸乙酯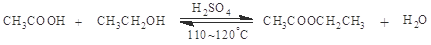

某化学兴趣小组的同学用以下装置进行该酯化反应的探究实验:
①要向大试管中加2mL浓硫酸、3mL乙醇、2mL乙酸,其具体操作是。
②小试管中装的是浓Na2CO3溶液,导气管不插入液面下是为了防止。
③相关物质的部分性质:
| 乙醇 |
乙酸 |
乙酸乙酯 |
|
| 沸点 |
78.0℃ |
117.9℃ |
77.5℃ |
| 水溶性 |
易溶 |
易溶 |
难溶 |
根据上表数据有同学提出可用水替代小试管中的Na2CO3溶液,你认为可行吗?说明理由:。④分离小试管中的乙酸乙酯应使用的仪器名称是;
⑤分离时,乙酸乙酯应该从仪器(填“下口放” 或“上口倒出”)。
⑥兴趣小组多次试验后,测出乙醇与乙酸用量和最后得到的乙酸乙酯生成量如下表:
| 实验序号 |
乙醇(mL) |
乙酸(mL) |
乙酸乙酯(mL) |
| a |
2 |
2 |
1.33 |
| b |
3 |
2 |
1.57 |
| c |
4 |
2 |
X |
| d |
5 |
2 |
1.76 |
| e |
2 |
3 |
1.55 |
表中数据X的范围是;实验a与实验e探究的目的是。