“白铁皮”具有较强的耐腐蚀性,是生产中常用的金属材料之一。镀锌层犹如铁皮的保护层,这层膜的厚度是判断镀层质量的重要指标。某研究性学习小组为了测定镀锌铁皮镀锌层的厚度,设计了下面的实验方案。
(1)讨论:在铁皮表面镀锌是为了 。(填字母)
a 锌没有铁活泼,镀在铁的表面可防止生锈
b 锌比铁活泼,并且在空气中容易形成致密的氧化膜,防止生锈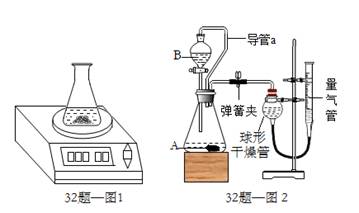
(2)甲同学的方案是:如图1,将镀锌铁皮浸泡在盐酸中,先用盐酸将镀锌铁皮表面的锌反应掉,通过测量因产生气体而形成差量计算出锌的质量,然后再计算得到锌层的厚度。但是乙同学回顾起上课时老师演示的“用足量盐酸除铁锈”的实验现象,马上对甲同学的方案的可行性提出了异议,乙同学的理由是 。
(3)乙同学查阅资料:ZnCl2、FeCl2都能与NaOH溶液反应,生成难溶于水Zn(OH)2和
Fe(OH)2,而Zn(OH)2既可以溶于酸也可以溶于碱,Fe(OH)2则只能溶于酸,于是设计了如下方案: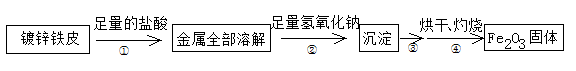
步骤②中加入足量氢氧化钠的目的是 。
(4)丙同学设计通过测量镀锌铁皮与酸反应产生气体的体积来计算锌层的厚度,他设计了如图2所示装置。其中仪器A中盛放的是镀锌铁皮,仪器B中盛放的是稀硫酸。
①选择用稀硫酸而不用浓盐酸的原因是 。
②检查量气装置气密性:连接好装置,关闭弹簧夹,从量气管注水,若观察到 ,说明该量气装置气密性良好。
③若分液漏斗上方不连接导管a,则测出气体体积会 (选填“偏小”、“偏大”或“没有影响”)。
水是生命之源,“珍惜水、节约水、保护水”是每个公民的义务和责任。
(1)下列“水”属于纯净物的是(填序号)。
A、蒸馏水 B、河水 C、自来水
(2)用如图甲装置进行电解水的实验,b中收集到的气体是,该实验说明水是由组成的。
(3)某同学自制如图乙所示简易净水器,图中活性炭的主要作用是 。
(4)高铁酸钾(K2FeO4)是一种新型、高效的多功能水处理剂。高铁酸钾受热时发生的反应为:4K2FeO4 2R+4K2O+3O2↑,则R是(填化学式)。
2R+4K2O+3O2↑,则R是(填化学式)。
(5)请举一例生活中节约用水的具体措施。
如图中A、B分别是某微粒的结构示意图,回答下列问题: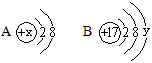
(1)若A是某阴离子的结构示意图,则x可能是下列中的____ (填序号)。
①8 ②10③11 ④12
(2)若B表示某原子的结构示意图,则y= _________ 。
(3)若A中x=12,则与B所形成化合物中,A的化合价是_____ 。
用化学用语表示:
(1)2个碳原子;
(2)2个镁离子;
(3)人体中含量最多的物质。
某快递公司违反国家规定快递有毒化学品,因化学品泄露,导致多人伤亡,被称为“夺命快递”。“夺命快递”中的化学品是氟乙酸甲酯(化学式为C3H5FO2),是有毒液体,在染料、医药、农药等工业领域有着广泛的用途。
(1)氟乙酸甲酯的相对分子质量是;
(2)氟乙酸甲酯中碳、氢、氟、氧的质量比是;
(3)有人说这“都是化学惹得祸”,你如何评价?。
学习化学离不开实验。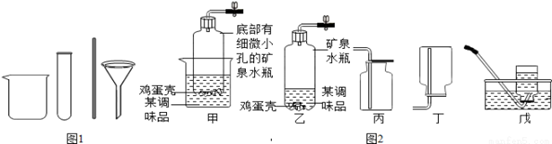
(1)小明同学在家里利用替代品进行相关实验。如:配制较多溶液时用玻璃杯代替如图1所示的仪器中的
(填仪器名称,下同);搅拌时用筷子代替。
(2)①写出实验室制取二氧化碳的化学方程式。
②小明同学选用片状的鸡蛋壳和(填一种厨房调味品)反应来制取二氧化碳,并利用矿泉水瓶、玻璃杯、橡皮塞、导管、止水夹等组装了如图2所示甲、乙气体发生装置.比较甲、乙装置,甲装置的优点是(填序号)。
A.反应过程中可以添加固体药品
B.可以控制反应的发生与停止
③选用甲装置可以进行的实验是(填序号)。
A.块状的胡萝卜与过氧化氢溶液制氧气B.加热高锰酸钾固体制氧气
C.粉末状的锌与稀硫酸制氢气D.浓硫酸与甲酸共热制一氧化碳
④收集二氧化碳常选用装置(填编号,下同);若收集氨气应选用装置(已知氨气极易溶于水,密度比空气小)。
⑤下列哪些方法可检验二氧化碳已收集满(填序号)。
A.将点燃的木条伸至集气瓶中部B.将湿润的蓝色石蕊试纸伸至集气瓶口
C.将点燃的木条伸至集气瓶口 D.将带火星的木条伸至集气瓶口