二十一世纪是海洋开发与利用的世纪,某市规划确立了“蓝色经济”发展战略,海洋化学资源的综合利用将是重点发展领域之一。以下是某研究性学习小组在探究海水综合利用中遇到的问题,请你参与探究:
问题一、海水制镁过程中如何富集镁离子?
甲、乙、丙三位同学各自提出自己的设想:
甲:直接往海水中加入石灰乳。
乙:高温加热蒸发海水后,加入石灰乳。
丙:向晒盐后的卤水中,加入石灰乳。
通过分析比较,你认为___________的设想最为经济合理(选填“甲”、“乙”或“丙”)。
问题二、粗盐提纯过程中如何除去可溶性杂质?
【查阅资料】
粗盐中含有硫酸钠、氯化钙等可溶性杂质。
【设计实验】
提纯时,先向粗盐水中加过量的氢氧化钡溶液,目的是_____①________;再加过量的____②______,除尽杂质阳离子;滤去沉淀,向滤液中加入__③_____,将溶液的pH调为7,即得到精盐水。
问题三、海水“制碱” 的产物成分是什么?
同学们从某企业取回少量碳酸氢钠受热完全分解后的固体样品,为确定其成分,进行
了如下探究:
【提出猜想】
甲的猜想:样品中只含有碳酸钠;
乙的猜想:样品中只含有氢氧化钠;
丙的猜想:样品中含有碳酸钠和氢氧化钠。
他们做出上述三种猜想的科学依据是________________________________。
【实验、记录与分析】
| 步骤 |
实验操作 |
实验现象 |
结论 |
| 1 |
取少量样品于试管中,加水完全 溶解,再加入________________ |
_____________________ |
乙的猜想 不成立 |
| 2 |
取步骤1反应后的溶液于试管中 ___________________________ |
无明显现象 |
只有甲的 猜想成立 |
【实验结论】
海水“制碱”的最终固体产物是碳酸钠。
【数据分析】
在取回的样品中加入200g7.3%的稀盐酸,恰好完全反应,请计算同学们带回了多少克固体样品?(要求有解题过程)
现将下列物质进行加热:①10g氯酸钾②3g二氧化锰③10g氯酸钾和3g二氧化锰的混合物④10g氯酸钾和3g高锰酸钾的混合物,反应完毕后,请问: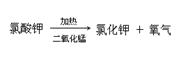
(1)用序号填写:产生氧气最多的是_______,不产生氧气的是________,产生氧气速度最慢的是.
(2)上述③中药品反应完毕后,试管内残留的两种固体__________________(填写物质名称)
现有氯酸钾、二氧化锰、锌粒、稀硫酸、氧化铜等药品,请利用所给的药品结合下列实验装置图回答问题.(收集装置不能重复使用)
A  B
B  C
C 
D  E
E F
F 
(1)写出实验室制取氧气的文字表达式______________________;制取氧气应选用的装置是_______和_______。(填字母)
(2)实验室制取氢气应选用的装置是_________和_________。(填字母)
(3)实验室中一般用铜与浓硝酸在常温下反应迅速产生二氧化氮气体。二氧化氮气体比氧气密度大,易溶于水。试用你学过的实验室制氧气和制氢气的知识回答:实验室用于制二氧化氮气体的发生装置可用(填序号)_________,收集二氧化氮气体的装置为_________
如下图所示,实验室用过氧化氢溶液和二氧化锰制取氧气,实验的相关数据如下表。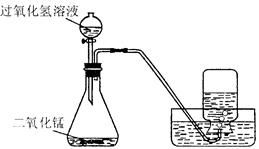
| 气体发生装置内物质的总质量 |
|
| 反应前 |
35.6 g |
| 反应后 |
34. 8 g |
(l)实验中检查该装置气密性的方法是________________________________ 。
(2)实验中集气瓶收集满氧气的现象是________________________________。
(3)反应生成氧气的质量为:_______________ g 。
实验室按下图所示装置制取CO2,并检验CO2的性质.试回答以下问题:
(1)实验室用装置A来制取CO2,常用的药品是____________和____________,写出两物质制取二氧化碳的化学反应方程式______________________________
(2)若要用装置B鉴定CO2,在B中应盛放的试剂名称是____________,当将标①和②的导管口连接时,B中看到的实验现象是____________________。
(3)若要用装置C证明CO2能与水反应生成碳酸,C中除有少量水外,应加入的试剂是_________________,当将标①和③的导管口连接时,C中看到的实验现象是________________。
(4)烧杯D中放有燃着的蜡烛如图所示,当将标①和④的导管口连接时,D中看到的实验现象是____________________________________。
请你参与下列探究:
【问题情景】在课外活动中,小斌按照课本实验(见图1)探究微粒的性质时,闻到了刺激性的氨味,于是,小斌在老师的指导下,设计了如图2的实验装置,进行同样的实验,结果不再有刺激性的氨味,并且快速出现实验现象,得到了和课本实验同样的结论。
【实验探究与结论】小斌用图2装置进行实验。
(1)滴入少量浓氨水后,湿润的酚酞滤纸条发生的变化是;从微观角度分析,此现象可说明的结论是。
(2)“图2的实验装置,快速出现实验现象”说明固体氢氧化钠遇到浓氨水时可能会
(填“放热”或“吸热”)。
(3)和课本实验比较,小斌改进后的装置的优点是(写出两点)
①;②。
【思维拓展】小媚受小斌实验的启发,将图2装置进一步改装成图3装置,用于验证二氧化碳的性质。
(1)打开活塞K滴入稀盐酸后,小试管中发生的反应的文字表达式为,发现两条用紫色石蕊试液润湿的试纸都变红,请你分析两条试纸变红的情况是。
| A.下面先变红,上面后变红 | B.上面和下面一起变红 |
| C.上面先变红,下面后变红 | D.以上均有可能 |
小媚从课本实验中知道,二氧化碳和水本身都不能使石蕊变色,因而她认为以上两个变化可验证的二氧化碳的性质是、。
(2)小柔认为小媚的装置还可以验证:①二氧化碳能使澄清石灰水变混浊;②二氧化碳不能燃烧,也不支持燃烧。小柔为完成自己的两个验证实验,对小媚的实验进行的简单改进:验证①、验证②。