氯碱工业常利用阳离子交换膜电解食盐水,下列说法不正确的是
| A.随着电解的进行,c(NaCl)降低,需不断补充饱和食盐水 |
| B.电解过程中采用增大阳极区溶液pH的方法,可以减少Cl2在水中的溶解量 |
| C.阳离子交换膜的作用是阻止OH-移向阳极,以使氢氧化钠在阴极区富集 |
| D.阳极表面用钛氧化物涂层处理,目的是降低电解产物Cl2对电极的腐蚀 |
在pH=1的溶液中,可以大量共存的离子是()
A.K 、Na 、Na 、SO 、SO 、S 、S O O |
B.NH 、Mg 、Mg 、SO 、SO 、Cl 、Cl |
C.Na 、K 、K 、HCO 、HCO 、Cl 、Cl |
D.K 、Na 、Na 、AlO 、AlO 、NO 、NO |
为维持人体内电解质平衡,人在大量出汗后应及时补充的离子是()
A.Mg |
B.Ca |
C.Na |
D.Fe |
含8.0 g NaOH的溶液中通入一定量H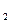 S后,将得到的溶液小心蒸干,称得无水物7.9 g,则该无水物中一定含有的物质是()
S后,将得到的溶液小心蒸干,称得无水物7.9 g,则该无水物中一定含有的物质是()
A.Na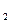 S S |
B.NaHS |
C.Na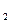 S和NaHS S和NaHS |
D.NaOH和NaHS |
在托盘天平的两个托盘中均放有一只盛有足量稀H2SO4的烧杯,调节天平使之平衡,向右边烧杯加入6.2 g Na2O,欲使天平平衡,应向左边的烧杯中加入()
| A.6.2 g Na2O2 | B.7.8 g Na2O2 |
| C.8 g NaOH | D.10.6 g Na2CO3 |
已知钡的金属活动性处于钾和钠之间。下列反应可以实现的是()
| A.钡可以从氯化钾溶液中置换出钾 | B.钡可以从冷水中置换出氢而得到氢气 |
| C.钡可以从氯化钠溶液中置换出钠 | D.可将Ba(OH)2加热制得BaO |