固体粉末X中可能含有Fe、Fe2O3、K2SiO3、K2SO3、KAlO2、MgCl2、K2CO3中的若干种。为确定该固体粉末的成分,现取X进行连续实验,实验过程及产物如下: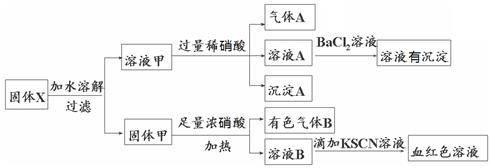
根据上述实验,以下说法正确的是
| A.气体A一定只是NO |
| B.由于在溶液A中加入BaCl2溶液有沉淀产生,因此可以判断溶液甲中含有K2SO3 |
| C.若向固体甲中加入足量浓盐酸,再加KSCN溶液,没有血红色,则证明原混合物中一定没有Fe2O3 |
| D.溶液甲中一定含有K2SiO3、可能含有KAlO2、MgCl2 |
几种短周期元素的原子半径及主要化合价如下表:
| 元素代号 |
X |
Y |
Z |
W |
| 原子半径/pm |
160 |
143 |
70 |
66 |
| 主要化合价 |
+2 |
+3 |
+5、+3、-3 |
-2 |
下列叙述正确的是
A.X、Y元素的金属性X<Y
B.一定条件下,Z单质与W的常见单质直接生成ZW2
C.Y的最高价氧化物对应的水化物能溶于稀氨水
D.四种元素形成的单核离子半径由大到小的顺序为Z3->W2->X2+>Y3+
已知:①钾比水轻;②钾的熔点低;③钾与水反应时要放出热量;④钾与水反应后溶液呈碱性。某学生将一块金属钾投入滴有酚酞试液的水中,该实验能证明四点性质中的
| A.①④ | B.①②④ | C.①③④ | D.①②③④ |
下列关于反应速率的说法正确的是
| A.v=0.10 mol·L-1·s-1是指1 s内某物质的物质的量浓度为0.10 mol·L-1 |
| B.对于任何化学反应来说,反应速率越快,反应现象就越明显 |
| C.化学反应速率只是对可逆反应才适用 |
| D.根据反应速率的大小,可以知道反应进行的相对快慢 |
下列说法中错误的是
| A.原子及其离子的核外电子层数等于该元素所在的周期数 |
| B.元素周期表中从ⅢB族到ⅡB族10个纵列的元素都是金属元素 |
| C.除氦外的稀有气体原子的最外层电子数都是8 |
| D.同一元素的各种同位素化学性质几乎完全相同 |
在恒温下的密闭容器中,有可逆反应:2NO(g)+O2(g) 2NO2(g)(反应放热),能说明已达到平衡状态的是
2NO2(g)(反应放热),能说明已达到平衡状态的是
| A.正反应生成NO2的速率和逆反应生成O2的速率相等 |
| B.N2O4和NO2的浓度相等 |
| C.混合气体的颜色保持不变 |
| D.单位时间内生成1mol O2的同时,生成1molNO |