(6分)铜是人类最早利用的金属之一。
(1)下列铜制品中,利用金属导热性的是 (填字母序号)。
A.铜质奖牌 B.铜导线 C.铜火锅
(2)验证铜、银的活动性,可以选用的试剂是 。
(3)利用废旧电池铜帽(含Cu、Zn)制取海绵铜(Cu),并得到硫酸锌溶液,主要流 程如下(反应条件已略去): 已知:2Cu+2H2SO4+O2△2CuSO4+2H2O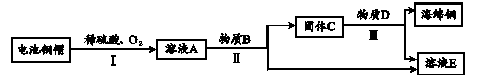
① 过程Ⅱ中分离操作的名称是 。
② 过程Ⅲ中有气体产生,反应的化学方程式为 。
溶液A中一定含有的溶质的物质有 。
分类是学习和研究物质及变化的常用方法。将氯化钾、氮气、氢氧化钾、硝酸、三氧化硫五种物质分类,填写在对应的位置上(写化学式)。
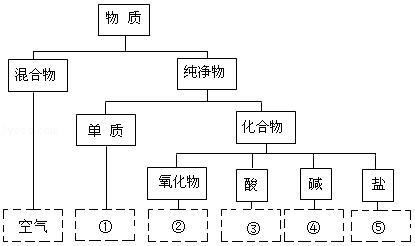
① ② ③ ④ ⑤
化学就在我们身边。从①熟石灰②金刚石③氯化钠④干冰四种物质中,选择适当的物质填空(填序号)。
(1)用于炒菜调味的是 ;
(2)用于人工降雨的是 ;
(3)用来裁玻璃的是 ;
(4)来改良酸性土壤的是 。
化学是在分子、原子层次上研究物质的科学。
(1)构成物质的粒子有分子、原子和 。
(2)如图为三种元素的原子结构示意图。
①氧原子在化学反应中容易 电子 (填“得到”或“失去”)。
②二氧化硫和二氧化碳都能与氢氧化钠溶液反应生成盐和水,将二氧化硫气体通入氢氧化钠溶液中生成亚硫酸钠(Na2SO3) 和水,写出该反应的化学方程式 。
③硒元素能增强人体免疫力,延缓衰老,山药等食物中常含硒元素。硒(Se)在氧气中燃烧生成二氧化硒。回答下列问题:
A.硒原子的核电荷数为 。
B.硒元素与氧、硫元素的化学性质相似,原因是它们的原子 相同。
C.写出硒在氧气中燃烧反应的化学方程式 。

生活离不开水,我们可以从组成、结构、性质等角度认识水。
(1)组成:如图所示电解水的实验中,试管a、b中产生气体的体积比约为 ,该实验证明水是由 组成的。
(2)结构:每个水分子是由 构成的。
(3)性质:水能与许多物质发生化学反应,写出水与氧化钙反应的化学方程式 。

化学就在我们身边,一些物质在生产生活中有重要的用途。现有①二氧化碳 ②活性炭 ③氮气 ④熟石灰 ⑤硝酸钾⑥不锈钢,选择适当的物质填空(填序号)。
(1)可用于冰箱除味剂的是 ;
(2)绿色植物进行光合作用吸收的是 ;
(3)与硫酸铜溶液混合可配成波尔多液的是 ;
(4)可充入食品包装袋中以防腐的是 ;
(5)可用于制造炊具的是 ;
(6)属于复合肥料的是 。