a、b、c、d、e分别是Cu、Ag、Fe、Al、Mg五种金属中的一种。已知:①a、c皆能与稀硫酸反应放出气体;②b与d的硝酸盐反应,置换出单质d;③c与强碱反应放出气体;④c、e在冷浓硫酸中发生钝化。由此可判断a、b、c、d、e依次为
| A.Fe Cu Al Ag Mg | B.Al Cu Mg Ag Fe |
| C.Mg Cu Al Ag Fe | D.Mg Ag Al Cu Fe |
离子反应是中学化学中重要的反应类型,在发生离子反应的反应物或生成物中,一定存在:①单质;②氧化物;③电解质;④盐;⑤化合物
| A.①② | B.③⑤ | C.④⑤ | D.①②④ |
下列物质中主要成分不是二氧化硅的是
| A.硅胶 | B.水晶 | C.玛瑙 | D.硅石 |
下列有关说法正确的是
| A.1 mol Cl2参加反应转移电子数一定为2NA |
B.在反应KIO3+6HI KI+3I2+3H2O中,每生成3 mol I2转移的电子数为6NA KI+3I2+3H2O中,每生成3 mol I2转移的电子数为6NA |
C.根据反应中HNO3(稀)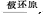 NO,而HNO3(浓) NO,而HNO3(浓)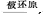 NO2可知,氧化性HNO3(稀)>HNO3(浓) NO2可知,氧化性HNO3(稀)>HNO3(浓) |
| D.含有大量NO3—的溶液中,不能同时大量存在H+、Fe2+、Cl- |
短周期元素W、X、Y、Z在元素周期表中的位置关系如图所示。下列说法正确的是
| A.元素Y的最高价氧化物对应水化物的酸性比Z的强 |
| B.元素Z一定位于元素周期表的第3周期第ⅦA族 |
| C.原子半径的大小顺序为rY>rW>rX |
| D.元素X可能为硼或碳或氮 |
下列说法正确的是
| A.SiO2能和水发生化合反应生成硅酸 | B.SiO2是酸性氧化物,它不溶于任何酸 |
| C.SiO2的俗名叫水玻璃,不溶于水 | D.SiO2又叫水晶,能溶于NaOH溶液中 |