X、Y、Z为三种气体,把a mol X和b mol Y充入一密闭容器中,发生反应X+2Y 2Z,达到平衡时,若它们的物质的量满足:n(X)+n(Y)=n(Z),则Y的转化率为 ( )
2Z,达到平衡时,若它们的物质的量满足:n(X)+n(Y)=n(Z),则Y的转化率为 ( )
A. ×100% ×100% |
B.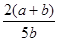 ×100% ×100% |
C. ×100% ×100% |
D. ×100% ×100% |
下列实验操作或结论正确的是( )
| A.配制溶液的操作中,转移溶液后,玻璃棒、烧杯未洗涤会使得所配溶液浓度偏高 |
| B.洗涤沉淀的操作是将沉淀置于过滤器中,边用玻璃棒搅拌边加蒸馏水冲洗 |
| C.实验室配制950 mL 0.2 mol/L的CuSO4溶液时,需称取胆矾的质量为50.0 g |
| D.制备Fe(OH)3胶体时,将饱和的FeCl3溶液滴入沸水中,边加热边搅拌,直到得到红褐色溶液 |
常温下,下列各组物质不能用一种试剂通过化学反应区别的是( )
| A.苯 乙酸乙酯 乙醇 | B.AgNO3 KNO3 Na2CO3 |
| C.MnO2 CuO FeO | D.(NH4)2SO4 K2SO4 NH4Cl |
下列离子方程式正确的是( )
| A.向漂白粉溶液中通入少量SO2气体:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO |
| B.将Na2O2固体投入H218O中:2Na2O2+2H218O=4Na++4OH-+18O2↑ |
| C.向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液,恰好使SO完全沉淀: NH+Al3++2SO+2Ba2++4OH-= Al(OH)3↓+NH3·H2O+2BaSO4↓ |
| D.Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-=2Fe2++I2 |
NA代表阿伏加德罗常数,下列有关叙述错误的是( )
| A.56 g铁粉在1mol氯气中充分燃烧,失去的电子数为3NA | |
B.标准状况下22.4升CH4和C2H4的混合气体所含氢原子数为4NA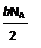 |
C.常温常压下,3.4gNH3中含N—H键数目为0.6NA |
| D.CO2通过足量Na2O2使固体增重bg时,反应中转移的电子数为 |
下列除杂方法正确的是( )
① 除去乙烷中少量的乙烯:通过酸性高锰酸钾溶液,洗气;
② 除去KNO3中少量的NaCl:溶解,蒸发浓缩,冷却结晶、过滤、干燥;
③ 除去CO2中少量的CO:在空气中点燃;
④ 除去苯中少量的苯酚:加入适量NaOH溶液,分液。
| A.①② | B.②④ | C.③④ | D.②③ |