在学习盐的性质时,某组同学将碳酸钠溶液和一瓶标签破损的溶液M(如图)
进行反应,有白色沉淀产生,过滤后得到澄清滤液。同学们对该实验进行了一系列的探究。
Ⅰ.定性探究:
探究一:M溶液中的溶质是什么?
(1)【提出猜想】该组同学认为M溶液的溶质有两种可能:
①是 ,
②是CaCl2.
【收集资料】CaCl2水溶液呈中性。
(2)【设计实验】同学们设计了如下方案并进行实验:
| 实验操作 |
实验现象 |
实验结论 |
| 取少量M溶液于试管中,向其中滴加 |
|
猜想①正确。碳酸钠与其反应的化学方程式为 |
探究二过滤后澄清滤液中会有哪些溶质?
【提出猜想】猜想一:NaOH 和Na2CO3 ;
猜想二: ;
猜想三:NaOH 。
(3)【实验验证】同学们经过交流讨论,设计以下实验方案确定滤液中溶质的组成:
| 实验操作 |
实验现象 |
实验结论 |
| 分别取少量滤液于A、B两支试管中,A中加入CaCl2溶液, B中加入 溶液 |
若A中产生白色沉淀,B中没有沉淀 |
“猜想一”成立 |
| |
“猜想二”成立 |
|
| |
“猜想三”成立 |
Ⅱ.定量探究:
【提出问题】过滤后澄清滤液中NaOH的质量分数是多少?
【设计实验】
小明同学取100g过滤后澄清滤液于烧杯中,向烧杯中逐滴加入过量的稀盐酸,产生的气体与所加入稀盐酸质量关系如下图所示:计算过滤后澄清滤液中NaOH的质量分数是多少?(请列出计算过程)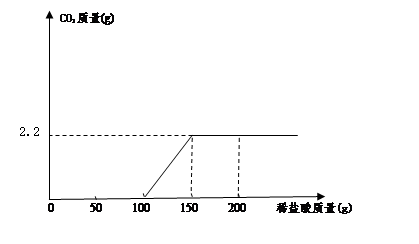
李老师在实验室制取了两瓶常见的无色气体,放置在试验台上,如下图所示。请回答下列问题:
(1)A气体可能是,推断的理由是。B气体可能是(写一种)。
(2)请设计实验验证所推断的B气体完成实验报告。
| 实验步骤 |
实验现象 |
实验结论 |
(3)在实验室制取B气体时,反应的化学方程式是,发生装置所需仪器的名称是。
为了比较我们呼出的气体和吸入的空气中二氧化碳含量的高低,某同学向盛满呼出气体的集气瓶内滴入数滴澄清的石灰水振荡(如下图A),他接下来所做的对比实验应选图 装置,你的理由是:。
为探究酒精灯火焰不同部位的加热效果,李明同学取来3支试管,分别编号为A、 B、 C。向试管内各加入 3 mL 水,进行了如下实验:
(1)把A试管底部放在酒精灯火焰上方约3 cm处加热;
(2)把B试管底部放在酒精灯外焰部分加热;
(3)把C试管底部放在酒精灯灯芯处加热。
实验结果如下表:
| 试管编号 |
A |
B |
C |
| 水沸腾所用时间(S) |
90 |
30 |
45 |
你由此得出的结论是,根据这一结论你对用酒精灯加热的建议是:。
填写实验报告:
| 实验现象 |
结论 |
| 把一只干燥的冷烧杯罩在酒精灯火焰上,观察到烧林内壁出现水雾 |
说明酒精燃烧时生成了 |
| 用手触摸上一步骤中的烧杯底部,感觉 |
说明酒精燃烧时有 放出 |
| 用塑料软管向一杯盛有澄清石灰水的烧杯内吹气,发现石灰水变浑浊 |
说明呼出的气体中含有 |
为证明某空杯内充满着空气,小红同学把杯口向下使杯子浸没在盛水的盆里,她将观察到的现象是。你还能用其他方法证明空杯内充满着空气吗?请简述操作方法和现象:
你如何证明空气中有二氧化碳?