某化学实验活动小组的同学为了探究实验室中久置的氢氧化钠固体的成分,进行了有关实验。请你参与他们进行的探究活动:
【提出问题】久置氢氧化钠固体的成分是什么?
【猜想与假设】
猜想Ⅰ:全部是NaOH;猜想Ⅱ:全部是Na2CO3;猜想Ⅲ: 。
【实验与探究】
(1)实验如下:
| 实验操作步骤 |
实验现象 |
结论及解释 |
| 步骤一:取少量固体样品于试管中,加蒸馏水完全溶解,然后加入足量的稀盐酸。 |
实验过程中始终没有气泡产生。 |
则证明猜想 成立。 |
| 步骤二:另取少量固体样品于试管中,加蒸馏水完全溶解,然后滴加氯化钡溶液。 |
实验过程中产生 。 |
则证明猜想Ⅱ或Ⅲ成立。 |
(2)为了进一步的验证猜想结果,小明同学提出如下实验方案:继续步骤二的实验,过滤,然后向滤液中滴加无色酚酞试液,若酚酞变红,则猜想Ⅲ成立;若酚酞不变红,则猜想Ⅱ成立。
小华同学立即对小明同学的方案提出了质疑,通过查阅资料知道,氯化钡溶液呈中性,不能使无色酚酞试液变红,但碳酸钠溶液呈 性(填“酸”或“碱”),能使酚酞变红,因此他认为该方案的操作步骤中应该改进的是 。
【反思与交流】久置的固体氢氧化钠变质的原因是(用化学方程式表示) 。
以下是氯化钠溶液的配制和粗盐中难溶性杂质的去除(需要计算粗盐的产率)实验活动中的部分操作。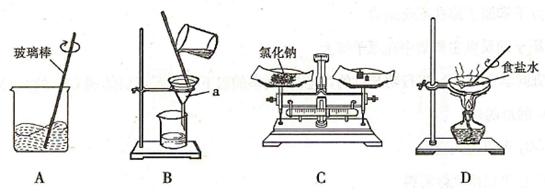
(1)仪器
的名称是。
(2)配制6%的氯化钠溶液和粗盐中难溶性杂质的去除都要用到的实验操作是(填序号)。
(3)
中玻璃棒搅拌的作用是使氯化钠。如果
中的滤液仍然浑浊,就应该。
操作中,当观察到蒸发皿中出现时,停止加热。
对比学习有利于发现事物的共性与个性.为探究酸的性质,同学们进行了如下实验.
| 实验内容 |
实验现象 |
分析与结论 |
 |
醋酸晶体试管内 (1),醋酸溶液试管中镁带表面冒气泡. |
酸的很多反应通常在水溶液中才能完成. |
用玻璃棒蘸硫酸在白纸上写字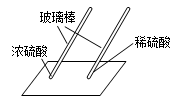 |
(2) (填"浓"或"稀")硫酸使白纸炭化. |
即使是同种酸,由于 (3)不同,它们的性质不完全相同. |
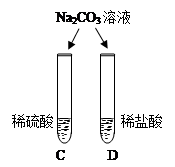 |
两试管中均产生 (4) |
不同的酸具有相似的性质,这是因为酸的组成中都含有(5)(填元素符号). |
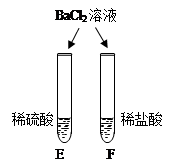 |
试管中产生 (6), 试管中无明显现象. |
不同的酸根会导致酸的"个性"差异.因此,可用氯化钡溶液鉴别盐酸和硫酸. |
清洗试管时,小乔同学将
两试管中的无色液体同时倒入一个洁净的废液缸,废液缸中立刻冒气泡并出现白色沉淀.请分析上述现象并回答:
Ⅰ.废液缸中产生气体的化学方程式为(7).
Ⅱ.废液缸里最终产生的白色沉淀中一定有硫酸钡,可能有(8)(填化学式).
实验室常利用以下装置完成气体制备及性质实验。请回答:
(1)指出编号仪器的名称:①,②。
(2)以上(从A-E中选择)装置有一处明显的错误,请加以改正。利用改正后的装置继续完成后面的实验。
(3)欲使用高锰酸钾制取氧气,应选择的发生装置是(填字母),反应原理用化学方程式表示为;为防止高锰酸钾粉末进入导管,应采取的措施是;若使用C装置收集氧气,实验结束时,应先从水槽中移出导气管,再熄灭酒精灯,原因是。
(4)将
和
的混合气体通过F装置(液体药品均足量),实验开始时关闭活塞b,打开活塞a,广口瓶中观察到的现象是,此时从导管c逸出的气体主要是。一段时间后,再关闭活塞a,打开活塞b,将分液漏斗中的稀盐酸滴入广口瓶中,此时逸出的气体主要是,反应原理用化学方程式表示为,欲收集该气体,应选择的装置是(填字母),验满的方法是。
下列是初中化学中的一些重要实验。请回答:
(1)
是氢气或甲烷的燃烧实验,点燃前必须;
(2)
实验中能够说明盐酸与氢氧化钠发生了反应的现象是;
(3)
是除去粗盐中难溶性杂质实验中的过滤操作,其中玻璃棒的作用是;过滤后发现滤液仍然浑浊,其可能的原因是(答出一种原因即可)。
某学习小组在如图所示的化学药品柜中发现一瓶标签模糊不清的无色溶液,已知这瓶溶液是以下5瓶溶液中的一种:
溶液、
溶液、
溶液、
溶液、
溶液。
(1)根据上述信息判断,该无色溶液不可能是溶液和溶液,只可能是其他3种溶液中的一种。
(2)为了进一步确定该溶液是何种溶液,请你设计实验方案,叙述实
验操作、预期现象与结论。
限用试剂:稀
、
溶液、
溶液、酚酞溶液
| 实验操作 |
预期现象与结论 |