Favorskii反应是化工生产中的重要反应,它是利用炔烃与羰基化合物在强碱性下发生反应,得到炔醇,反应原理为: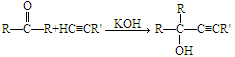
已知:
以下合成路线是某化工厂生产流程的一部分:
请回答下列问题:
(1)写出F中官能团的名称 。
(2)写出D的名称(系统命名) 。
(3)④的反应类型是 ;B的结构简式是 。
(4)写出反应⑥的化学方程式为 。
(5)H是D的同分异构体,核磁共振氢谱有3种峰且属于炔烃的结构简式为
、 。
(6)有关C的说法正确的是
| A.能使溴的四氯化碳溶液褪色 | B.能和氢氧化钠溶液反应 |
| C.能使酸性高锰酸钾褪色 | D.能与乙酸发生酯化反应 |
(10分)现有A、B、C、D四种可溶性盐,它们的阳离子分别可能是Ba2+、Ag+、Na+、Cu2+中的某一种,阴离子则可能是NO3-, SO42-, Cl-,CO32-离子中的某一种。
(1)若把四种盐溶解在四支试管中,只有C盐溶液呈蓝色。
(2)若向(1)的四支试管中分别加入盐酸,B盐溶液中有沉淀生成,D盐溶液中有无色无味气体放出。
根据以上实验事实推断它们的化学式为:ABCD
写出B盐与盐酸反应的离子方程式
甲乙两人分别用不同的方法配制100mL 0.92 mol/L的稀硫酸。
⑴甲:量取mL98﹪密度为1.84g/cm3的浓硫酸,小心地倒入成有少量水的烧杯中,搅拌均匀再转移到100mL容量瓶中,用少量的水将烧杯玻璃棒洗涤2-3次,将每次洗涤液也转移到容量瓶中,然后小心地向容量瓶中加水 定容,塞好瓶塞,反复上下摇匀。
定容,塞好瓶塞,反复上下摇匀。
①将溶液转移到容量瓶中的正确操作是
;
②定容的正确操作是。
⑵乙:用100mL量筒量取所需体积的浓硫酸,并向其中小心地加入少量的水,均匀搅拌待冷却至室温后,再加入水至100mL刻度线,再搅拌均匀。
你认为此法是否正确?若不正确,指出其中的错误之处
。
(12分)利用如下图的装置来做下面的实验: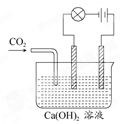
(1)先在玻璃容器里盛半杯Ca(OH)2溶液,然后由导管向容器溶液里通入CO2气体。随着CO2的通入,电灯就渐渐变暗,通入一定量时,电灯几乎完全熄灭,原因是 __________________________,如果继续通入CO2气体,电灯又会逐渐亮起来,原因是__________________________。在通入CO2的同时,能观察到溶液发生的现象是________________________,有关反应的离子方程式为_________________________。
(2)如果用氯化氢气体代替CO2气体,则观察到灯泡亮度变化是_________。有关离子反应方程式____________。
现有下列四种物质:Na2SO4、BaSO4、蔗糖(C12H22O11)、H2SO4,按照一定的依据,能找出一种物质与其它三种物质不同,从而分成两类。请你试试看,一共能找出多少种分法,把分类的依据和结果写在下面(至少填三种)
| 与其它三种不同的物质 |
分类依据 |
⑴通常状况下,甲同学取1 mol H2O加热到100℃时,液态水会汽化为水蒸气(如图所示),该过程属于变化。
在保持压强不变的情况下,水蒸气的体积22.4L 。(填“>”、“<”或“=”)
⑵乙同学做H2在O2中燃烧的实验,该实验过程属于变化,
在该变化过程中,一定保持相等的是(填序号)。
| A.反应物分子数目与生成物分子数目 |
| B.反应物原子总物质的量与生成物原子总物质的量 |
| C.反应物总质量与生成物总质量 |
| D.反应物体积与生成物体积 |