根据下图判断,下列说法不正确的是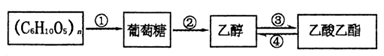
| A.(C6H10O5)n可表示淀粉或纤维素 |
B.反应②化学方程式为C6H12O6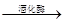 2C2H5OH+2CO2 2C2H5OH+2CO2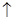 |
| C.反应③得到的乙酸乙酯中含有乙醇和乙酸,可用饱和氢氧化钠溶液除去 |
| D.反应③和④都属于取代反应 |
关于氢键,下列说法正确的是
| A.H2S沸点比H2O低原因是水分子间易形成氢键 |
| B.氯化钠易溶于水是因为形成了氢键 |
| C.氨易液化与氨分子间存在氢键无关 |
| D.H2O是一种非常稳定的化合物,这是由于氢键所致 |
实验室用浓盐酸与二氧化锰反应制取氯气,下列有关说法中正确的是(气体体积在标准状况下测定)
| A.若提供0.4 mol HCl,MnO2不足量,则可制得氯气2.24 L |
| B.若提供0.4 mol HCl,MnO2过量,则可制得氯气2.24 L |
| C.若有0.4 mol HCl参与反应,则可制得氯气2.24 L |
| D.若有0.4 mol HCl被氧化,则可制得氯气2.24 L |
如图,电解用粗盐(含 、
、 、
、 等杂质)配制的食盐水,以下说法正确的是
等杂质)配制的食盐水,以下说法正确的是
| A.a是电解池的正极 | B.a电极上发生还原反应 |
| C.b电极附近有白色沉淀出现 | D.b电极上有黄绿色气体产生 |
为了证明(NH4)2Fe(SO4)2·6H2O(硫酸亚铁铵晶体)的成分中含有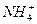 、
、 、
、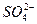 和H2O,下列实验叙述中不正确的是
和H2O,下列实验叙述中不正确的是
| A.取少量硫酸亚铁铵晶体放入试管,加热,试管口有液体生成,则可证明晶体的成分中含有结晶水 |
| B.硫酸亚铁铵晶体溶于水,得淡绿色溶液,滴入2滴KSCN溶液,溶液不显红色,再滴入几滴新制氯水,溶液变为红色,则可证明晶体的成分中含有Fe2+ |
C.硫酸亚铁铵晶体溶于水,加少量稀盐酸,无现象,再滴入几滴BaCl2溶液,有白色沉淀生成,则可证明晶体的成分中含有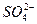 |
D.取少量硫酸亚铁铵晶体放入试管,加入少量稀NaOH溶 液,在试管口用湿润的红色石蕊试纸检验,则可证明晶体的成分中含有 液,在试管口用湿润的红色石蕊试纸检验,则可证明晶体的成分中含有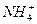 |
关于胶体和溶液的区别,下列叙述中正确的是
| A.溶液呈电中性,胶体带有电荷 |
| B.溶液中溶质微粒一定不带电,胶体中分散质微粒带有电荷 |
| C.溶液中分散质微粒能透过滤纸,胶体中分散质微粒不能透过滤纸 |
D.溶液中通过一束光线没有特殊现象,胶体中通过一束光线出现明亮的 光带 光带 |