(12分)Ⅰ.(1)AgNO3的水溶液呈 (填“酸”、“中”、“碱”)性,常温时的pH 7(填“>”、“=”、“<”),原因是(用离子方程式表示): ;实验室在配制AgNO3的溶液时,常将AgNO3固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,以 ________(填“促进”、“抑制”)其水解。
(2)在配制硫化钠溶液时,为了防止发生水解,可以加入少量的 。
Ⅱ. 已知水在25 ℃(A)和T ℃(B)时,其电离平衡曲线如图所示: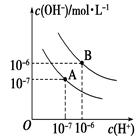
(1)25 ℃时,将pH=3 的H2SO4溶液与pH=10的NaOH溶液混合,若所得混合溶液的pH=7,则H2SO4溶液与NaOH溶液的体积比为 。
(2)T ℃时,若10体积pH1=a的某强酸溶液与1体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强Ⅰ碱的pH2之间应满足的关系是 。
(3)曲线B对应温度下,pH=3的HCl溶液和pH=9的某碱溶液等体积混合后,混合溶液的pH>7。请分析其原因: 。
(1)已知2 mol氢气燃烧生成液态水时放出572kJ热量,
① 该反应的生成物能量总和 (填“大于”、“小于”或“等于”)反应物能量总和。
② 若2mol氢气完全燃烧生成水蒸气,则放出的热量 (填“>”、“<”或“=”)572 kJ。
(2)FeS2焙烧产生的SO2可用于制硫酸。已知25℃、101 kPa时:
2SO2(g) +O2(g) 2SO3(g)△H1= -197 kJ/mol;①
2SO3(g)△H1= -197 kJ/mol;①
H2O (g) = H2O(1)△H2= -44 kJ/mol;②
2SO2(g)+O2(g)+2H2O(g) = 2H2SO4(l)△H3= -545 kJ/mol。③
则SO3 (g)与H2O(l)反应的热化学方程式是
[化学--修5:有机化学基础](15分)分别由C、H、O三种元素组成的有机物A、B、C互为同分异构体,它们分子中C、H、O元素的质量比为15︰2︰8,其中化合物A的质谱图如下。
A是直链结构,其核磁共振氢谱有三组峰,且峰面积之比为1︰1︰2,它能够发生银镜反应。B为五元环酯。C的红外光谱表明其分子中存在甲基。其它物质的转化关系如下:
已知:500℃时CH3-CH=CH2 + Cl2 → ClCH2-CH=CH2 + HCl
(1)A的分子式是:___________。A分子中的官能团名称是:___________。
(2)B和G的结构简式分别是:________、_________。
(3)写出下列反应方程式(有机物用结构简式表示)
A与银氨溶液反应:_____________;
G→H:___________________________;
(4)与I具有相同的官能团的同分异构体还有____________种,任写一种:。
[化学--修2:化学与技术](15分)
世界环保联盟建议全面禁止使用氯气用于饮用水的消毒,而建议采用高效“绿色”消毒剂二氧化氯。二氧化氯是一种极易爆炸的强氧化性气体,易溶于水、不稳定、呈黄绿色,在生产和使用时必须尽量用稀有气体进行稀释,同时需要避免光照、震动或加热。实验室以电解法制备ClO2的流程如下:
(1) ClO2中所有原子(填“是”或“不是”)都满足8电子结构。上图所示电解法制得的产物中杂质气体B能使石蕊试液显蓝色,除去杂质气体可选用
A.饱和食盐水 B.碱石灰 C.浓硫酸 D.蒸馏水
(2)稳定性二氧化氯是为推广二氧化氯而开发的新型产品,下列说法正确的是
A.二氧化氯可广泛用于工业和饮用水处理
B.应用在食品工业中能有效地延长食品贮藏期
C.稳定性二氧化氯的出现大大增加了二氧化氯的使用范围
D.在工作区和成品储藏室内,要有通风装置和监测及警报装置
(3) 欧洲国家主要采用氯酸钠氧化浓盐酸制备。化学反应方程式为。缺点主要是产率低、产品难以分离,还可能污染环境。
(4) 我国广泛采用经干燥空气稀释的氯气与固体亚氯酸钠(NaClO2)反应制备,化学方程式是,此法相比欧洲方法的优点是。
(5) 科学家又研究出了一种新的制备方法,利用硫酸酸化的草酸(H2C2O4)溶液还原氯酸钠,化学反应方程式为_______________________。此法提高了生产及储存、运输的安全性,原因是_________。
(1)某科研小组研究在其他条件不变的情况下,改变起始氢气物质的量[用n(H2)表示]对N2(g)+3H2(g) 2NH3(g)△H<0反应的影响,实验结果可表示成如下图所示的规律(图中T表示温度,n表示物质的量):
2NH3(g)△H<0反应的影响,实验结果可表示成如下图所示的规律(图中T表示温度,n表示物质的量):

①比较在a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是__________点。
②若容器容积为1L,若只加入反应物,当n=3mol时,反应达到平衡时N2、H2的转化率均为60%,此条件下(T2),反应的平衡常数K=_______________(精确到0.01)。
③图像中T2_________T1(填“高于”、“低于”、“等于”、“无法确定”)。
(2)氨气和氧气从145℃就开始反应,在不同温度和催化剂条件下生成不同产物(如图):
①4NH3(g)+5O2(g) 4NO(g)+6H2O(l) △H=-akJ·mol-1
4NO(g)+6H2O(l) △H=-akJ·mol-1
②4NH3(g)+3O2(g) 2N2(g)+6H2O (l) △H=-bkJ·mol-1
2N2(g)+6H2O (l) △H=-bkJ·mol-1
温度较低时以生成__________为主,温度高于900℃时,NO产率下降的原因是____________,写出汽车尾气产生NO的热化学方程式_____________________________________________。
(3)NO会继续快速被氧化为NO2,又已知:2NO2 (g) N2O4 (g)ΔH<0
N2O4 (g)ΔH<0
①现取五等份NO2,分别加入温度不同、容积相同的恒容密闭容器中,发生反应:2NO2(g) N2O4(g)。反应相同时间后,分别测定体系中NO2的百分含量(NO2%),并作出其随反应温度(T)变化的关系图。下列示意图中,可能与实验结果相符的是。
N2O4(g)。反应相同时间后,分别测定体系中NO2的百分含量(NO2%),并作出其随反应温度(T)变化的关系图。下列示意图中,可能与实验结果相符的是。
②保持温度体积不变,向上述平衡体系中再通入一定量的NO2,则达平衡时NO2的转化率(填增大、减小、不变、无法确定)。
X是一种新型无机非金属材料,具有耐磨、耐腐蚀、抗冷热冲击性。有关生产过程如下:
为了确定C的组成,某同学进行了以下的探究过程。已知F、G都是难溶于水和稀硝酸的白色沉淀,I可做光导纤维。
按要求回答下列问题:
(1)C的空间构型为;X的化学式为。
(2)反应②的化学方程式为。
(3)反应⑦的离子方程式。
(4)E是重要的工业原料,常见工业制备E的方法存在着一定的局限性,现在设想用电化学的方法制备E,并向外界提供电能,则正极反应式为______________________________,现将该电池与另一如图所示的蓄电池充电,该电池总反应式为:Pb+PbO2+4H++2SO42- 2PbSO4+2H2O,当制得2molE时,阳极质量__________(填“增重”或“减轻”) __________g。
2PbSO4+2H2O,当制得2molE时,阳极质量__________(填“增重”或“减轻”) __________g。