实验室常用的干燥剂“碱石灰”是CaO和固体NaOH的混合物,极易与空气中水蒸汽和CO2反应而变质。某同学对一瓶久置的“碱石灰”作了如下探究:
(1)猜想:
猜想Ⅰ:没有变质,“碱石灰”只含有CaO、固体NaOH;
猜想Ⅱ:已完全变质,“碱石灰”全部变成了CaCO3和Na2CO3。
则CaO与水反应的反应方程式为 。
(2)实验:如图所示:
(3)判断:
a. 若Ca(OH)2、CaCO3和Na2CO3投入到水中不会放热,则由操作②现象判断:猜想Ⅱ
(填:成立、不成立)
b. 操作④发生化学反应的方程式为 ;由操作⑤⑥的现象判断:滤液中含有
(写化学式);由此判断猜想Ⅰ (填:成立、不成立)。
c. 综合a和b的结论,判断该样品变质情况为 。
(4)拓展:由上述实验说明,实验室中“碱石灰”应 保存;操作③中玻棒的作用是 。
为了解决环境因素对维生素C含量的影响,从而更好地保存有关食物,某兴趣小组同学根据维生素C可使高锰酸钾(KMnO4)溶液褪色的原理,进行了如下表所示的实验。
| 编号 |
维生素C溶液的处理方法 |
使40毫升高锰酸钾(KMnO4)溶液褪色的滴数 |
| 1 |
放置于室内暗处0.5小时 |
15 |
| 2 |
阳光强烈直射5小时后,放置于室内暗处0.5小时 |
22 |
| 3 |
煮沸10分钟后,放置于室内暗处0.5小时 |
21 |
(1)他们探究了对维生素C含量的影响。
(2)他们的探究对我们的启示是:在贮存富含维生素C的食物时,应,以防止其中的维生素C过量流失,降低食物的营养价值。
(3)为了解维生素C的化学性质,他们用pH试纸测得该维生素C溶液的pH在1至2之间,说明维生素C具有性。
小明暑假期间到农田施肥时,发现撒落在地上的碳酸氢铵在阳光的照射下很快消失了,同时有浓烈的刺激性气味。他很好奇,返校后和同学们进行探究,请你一同参与。
【提出问题】温度较高时碳酸氢铵能分解吗?产物是什么?
【猜想假设】碳酸氢铵受热易分解,产物可能为水、二氧化碳、氨气。
【实验设计】小明设计了如图所示的装置进行实验(夹持装置省略)。
(1)根据现象:,证明实验后生成了水和氨气。
(2)装置B中澄清石灰水,证明产物中有二氧化碳生成。
(3)小红同学认为若将装置B中的澄清石灰水改为NaOH溶液,再通过实验验证
B中的产物,也可以证明碳酸氢铵分解后有二氧化碳生成。请你帮她设计并完成验证B中产物的实验。
【实验结论】碳酸氢铵受热易分解,其反应的化学方程式为。
【实验评价】在上述同学们的探究活动中,你最欣赏的是。
【实验反思】根据以上实验,你认为碳酸氢铵化肥在存放时应注意的问题是
。
某化学实验小组欲探究盐酸、氢氧化钙两种物质的化学性质,取8支试管分别用A~H编号后,做如下实验。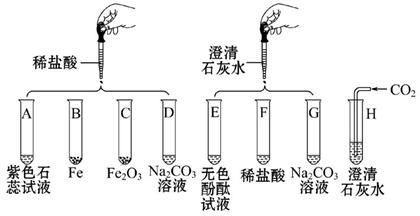
(1)实验中观察到有气泡出现的试管是,有沉淀生成的试管是。
(2)写出实验中无明显现象产生的试管中发生反应的化学方程式。
(3)实验后某试管中为红色溶液,当向其中加入过量的后,溶液变为蓝色。由此推断,该试管中最初盛有的物质是。
(4)实验后某试管的底部有白色固体,过滤后向滤液中滴加稀盐酸,一段时间后有气泡出现,则该滤液中的溶质是。
钢铁产业是我国的支柱产业之一,选择优质炼铁原料十分重要。甲、乙两组同学对某钢铁厂所购进的赤铁矿粉中主要成分Fe2O3的含量进行测定。(假设每步反应均能完全进行,赤铁矿粉中的杂质性质稳定,既不溶于水也不参与反应)
(1)甲组同学称取一定质量的赤铁矿粉,采用如图装置进行实验。
①装置A中发生反应的化学方程式是。
②为充分吸收反应生成的CO2,装置B中应盛放的试剂是浓溶液。
③可以通过下面不同的方法计算赤铁矿粉中Fe2O3的含量。
方法一:称量反应前后装置A的总质量,计算出Fe2O3的含量。
方法二:称量,得出反应生成的CO2的质量,计算出Fe2O3的含量。
(2)乙组同学称取等质量的赤铁矿粉放入烧杯中,向烧杯中加入过量的稀硫酸充分反应,(填一个操作名称)后立即称量。根据称量的数据计算出Fe2O3的含量。
(3)甲、乙两组同学通过相互比较后对各自的实验方案进行评价。
维生素C(简称Vc,又名抗坏血酸),易溶于水,易被氧化。人体缺乏Vc可能引发多种疾病。水果和蔬菜中含有丰富的Vc。某研究性学习小组对它探究如下:
探究一:测定饮料中Vc的含量。
【查阅资料】Vc能和高锰酸钾反应,使紫色的高锰酸钾溶液褪色。
【设计方案】分别向盛有1 mL等浓度高锰酸钾稀溶液的四支试管中逐滴滴加果味饮料、苹果汁、梨汁和0.04%的Vc溶液,边滴边振荡,直至高锰酸钾溶液褪色。
【实验数据】
【实验结论】分析数据可知,Vc含量最高的是,含量为(各液体密度上的差别和每一滴的体积差别忽略不计)。
探究二:蔬菜放置时间的长短对其Vc含量是否有影响。
【设计方案】请你用新鲜的黄瓜、放置一周的黄瓜、高锰酸钾稀溶液和必要的仪器设计实验方案:。
【实验结论】按上述方案实验,根据这一实验结果,分析得出蔬菜放置时间的长短对其Vc含量有影响。
【实验反思】化学实验需要控制变量。下列情况不会影响到测定结果的是。
| A.每次实验所用的果汁颜色不同 |
| B.量取的被测物质的体积不同 |
| C.试管的大小不同 |
| D.没有用同一规格胶头滴管滴加 |