已知化学平衡、电离平衡、水解平衡和溶解平衡均符合勒夏特列原理。请回答下列问题:
(1)可逆反应FeO(s)+CO(g) Fe(s)+CO2(g)是炼铁工业中一个重要反应,其温度与平衡常数K的关系如下表:
Fe(s)+CO2(g)是炼铁工业中一个重要反应,其温度与平衡常数K的关系如下表:
| T(K) |
938 |
1100 |
| K |
0.68 |
0.40 |
①写出该反应平衡常数的表达式__________。
②若该反应在体积固定的密闭容器中进行,在一定条件下达到平衡状态,若升高温度,混合气体的平均相对分子质量_____;充入氦气,混合气体的密度____(选填“增大”、“减小”、“不变”)。
(2)常温下,浓度均为0.1 mol·L-1的下列六种溶液的pH如下表:
| 溶质 |
CH3COONa |
NaHCO3 |
Na2CO3 |
NaClO |
NaCN |
C6H5ONa |
| pH |
8.8 |
9.7 |
11.6 |
10.3 |
11.1 |
11.3 |
①上述盐溶液中的阴离子,结合质子能力最强的是
②根据表中数据判断,浓度均为0.01 mol·L-1的下列五种物质的溶液中,酸性最强的是 ;
将各溶液分别稀释100倍,pH变化最小的是 (填编号)。
A.HCN B.HClO C.C6H5OH D.CH3COOH E.H2CO3
③据上表数据,请你判断下列反应不能成立的是 (填编号)。
A.CH3COOH+ Na2CO3=NaHCO3+CH3COONa B.CH3COOH+NaCN=CH3COONa+HCN
C.CO2+H2O+2NaClO=Na2CO3+2HClO D.CO2+H2O+2C6H5ONa=Na2CO3+2C6H5OH
④要增大氯水中HClO的浓度,可向氯水中加入少量的碳酸钠溶液,反应的离子方程式为
(3)已知常温下Cu(OH)2的Ksp=2×10-20。又知常温下某CuSO4溶液里c(Cu2+)=0.02 mol·L-1,如果要生成Cu(OH)2沉淀,则应调整溶液pH大于 ;要使0.2 mol·L-1的CuSO4溶液中Cu2+沉淀较为完全 ( 使Cu2+浓度降至原的千分之一)则应向溶液里加NaOH溶液,使溶液pH为 。
为除去粗盐中的Ca2+、Mg2+、Fe3+、SO以及泥沙等杂质,一位同学设计了一种制备精盐的实验方案,步骤如下(用于生成沉淀的试剂均稍过量):

(1) 判断BaCl2已过量的方法是______________________________。
(2) 第④步中,相关的离子方程式是_________________________________。
(3)蒸发、结晶时,当中剩余时停止加热。
根据反应8NH3 + 3Cl2 ="=" 6NH4Cl+ N2 ,回答下列问题:
(1) 还原剂是(写化学式);
(2) 用双线桥法表示该反应电子转移的方向和数目;
(3)当反应中转移1.806×1024个电子时,被氧化的气体在标准状况下的体积为升。
某中学环境监测兴趣小组的同学在一条鱼虾绝迹的小河边发现甲、乙、丙、丁四个工厂 ,如右图所示。这些工厂往小河里排放的废水中各含一种化合物。经检测发现:①甲处河水呈浅黄色;②乙处河水呈红褐色浑浊状;③丙处河水逐渐变澄清;④丁处河水不断冒气泡;⑤M处水样的pH大于7,加入足量的稀HNO3后再加入BaCl2溶液,无沉淀生成; ⑥N处水样的 pH小于7。请回答: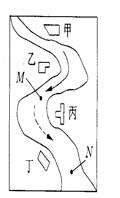
(1)四个工厂所排放的废水中,分别含有下列化合物中的哪种物质:
硫酸铁、氢氧化钠、硝酸银、碳酸钠、氯化铁、硫酸。
甲______,乙______,丙______,丁______。(均填化学式)
(2)写出丙、丁两处所发生反应的离子方程式:
丙_______________; 丁_______________。
四只失去标签的试剂瓶中分别盛有NaCl溶液、NaNO3溶液、Na2CO3溶液和Na2SO4溶液,就如何检验这四种溶液做如下实验:先用四只试管分别取四种溶液各1mL, ① 在四只试管中分别滴入过量的同一种试剂,根据反应现象检验出一种物质;② 在剩余的三只试管中分别滴入第二种试剂,又检验出一种物质;③ 在剩余的两只试管中分别滴入第三种试剂,检验出第三种物质;④在三次实验中都没有明显现象的是第四种物质。请回答:
(1)①中加入的试剂的名称是;
(2)②中检验出的物质是(写化学式);
(3)③中反应的现象是。
某同学将标准状况下44.8L的HCl气体溶于水,配成500mL的溶液,并取出100mL该盐酸溶液与2mol/L的Ba(OH)2溶液进行中和反应。
(1)根据公式,可知该HCl气体的物质的量为________。
(2)根据公式,可知所配成的盐酸溶液的物质的量浓度为。
(3)100mL盐酸溶液中含HCl的物质的量为,
(4)根据化学反应方程式,可知反应过程中n[Ba(OH)2]: n(HCl) =,所以n[Ba(OH)2]为mol,因此,反应所消耗的的体积Ba(OH)2为。