下列各组元素性质的递变情况中,错误的是
A.Li、Be、B原子的最外层电子数依次增多
B.P、S、Cl元素的最高正化合价依次增大
C.B、C、N、O、F的原子半径依次增大
D.Li、Na、K、Rb元素的金属性依次增强
实验室将9 g铝粉跟一定量的金属氧化物粉末混合形成铝热剂。发生铝热反应之后,所得固体中含金属单质为18 g,则该氧化物粉末可能是( )
①Fe2O3和MnO2②MnO2和V2O5③Cr2O3和V2O5④Fe3O4和FeO
| A.①② | B.②④ | C.①④ | D.②③ |
根据表中信息,判断下列叙述中正确的是
| 序号 |
氧化剂 |
还原剂 |
其它反应物 |
氧化产物 |
还原产物 |
| ① |
Cl2 |
FeBr2 |
/ |
Cl- |
|
| ② |
KClO3 |
浓盐酸 |
/ |
Cl2 |
|
| ③ |
KMnO4 |
H2O2 |
H2SO4 |
O2 |
Mn2+ |
A.表中①组的反应可能有一种或两种元素被氧化
B.氧化性强弱的比较: KClO3>Fe3+>Cl2>Br2
C.表中②组反应的还原产物是KCl,电子转移数目是6e-
D.表中③组反应的离子方程式为:2MnO4-+ 3H2O2 + 6H+=2Mn2+ + 4O2↑+ 6H2O
化学方程式可简明地体现元素及其化合物的性质。已知:
氧化还原反应:
2FeCl3 + 2HI = 2FeCl2 + I2 + 2HCl; 2Co(OH)3 + 6HCl = 2CoCl2 + Cl2↑ + 6H2O
2Fe(OH)2 + I2 + 2KOH= 2Fe(OH)3 + 2KI; 3I2 + 6KOH=" 5KI" + KIO3 + 3H2O
复分解反应:
2HSCN + K2CO3 =" 2KSCN" + CO2 ↑ + H2O; KCN + CO2 + H2O =" HCN" + KHCO3
热分解反应:
4NaClO 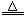 3NaCl + NaClO4;NaClO4
3NaCl + NaClO4;NaClO4 NaCl + 2O2↑
NaCl + 2O2↑
下列说法不正确是:
| A.氧化性(酸性溶液):FeCl3>Co(OH)3>I2 |
| B.还原性(碱性溶液):Fe(OH)2>I2>KIO3 |
| C.热稳定性:NaCl>NaClO4>NaClO |
| D.酸性(水溶液):HSCN>H2CO3>HCN |
下列叙述正确的是
① 7Li+中含有的中子数与电子数之比为2︰1
② 在C2H6分子中极性共价键与非极性共价键数之比为3︰1
③ 常温下,11.2 L的甲烷气体中含有的氢、碳原子数之比为4︰1
④ 5.6 g铁与足量的氯气反应失去的电子与参与反应的铁的物质的量之比为2︰1
| A.① ② | B.② ③ | C.① ③ | D.③ ④ |
NaCl是一种化工原料,可以制备一系列物质(如图)。下列说法正确的是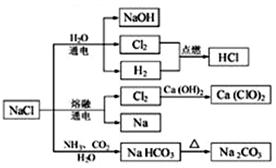
| A.25℃,NaHCO3在水中的溶解度比Na2CO3的大 |
| B.石灰乳与Cl2的反应中,Cl2既是氧化剂,又是还原剂 |
| C.常温下干燥的Cl2能用钢瓶贮运,所以Cl2不与铁反应 |
| D.如图所示转化反应都是氧化还原反应 |