下列关于物质结构、元素性质的说法正确的是
A.C2H6分子中既有σ键又有π键还有非极性键
B.C、P、S、Cl的最高价氧化物对应水化物的酸性逐渐增强
C.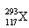 和
和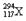 两种核素的核外电子数之差为1
两种核素的核外电子数之差为1
D.K、Al分别与不足量的稀盐酸反应所得溶液均呈中性
我国发射载人航天飞船用于火箭启动炸药的是氕化锂、氘化锂和氚化锂,它们
| A.都是共价化合物 |
| B.都具有较强还原性 |
| C.由同位素原子构成的同分异构体 |
| D.微粒的半径H-小于Li+ |
“地沟油”在一定条件下,能发生如下反应,化学方程式为:
下列叙述错误的是
| A.“地沟油”主要成分是高级脂肪酸的甘油酯 |
| B.生物柴油是不同酯组成的混合物 |
| C.生物柴油属于化石燃料 |
| D.“地沟油”可用于制备生物柴油 |
下列现象中,能用键能大小解释的是
| A.硝酸易挥发,而硫酸难挥发 | B.常温常压下,溴呈液态,碘呈固态 |
| C.稀有气体一般很难发生化学反应 | D.氮气的化学性质比氧气稳定 |
化学科学需要借助化学专用语言来描述,下列化学用语不正确的是
A.Cl-的结构示意图: |
B.羟基的电子式: |
| C.HClO的结构式:H—Cl—O |
D.原子核内有10个中子的氧原子: O O |
有关下列离子方程式的说法正确的是
| A.等物质的量MgCl2、Ba(OH)2和HCl溶液混合:Mg2++3OH-+H+=Mg(OH)2↓+H2O |
| B.向NaAlO2溶液中通入过量CO2的反应为:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- |
| C.等物质的量的FeBr2与Cl2反应为:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- |
| D.用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++5H2O2=2Mn2++5O2↑+8H2O |