我们每时每刻都生活在空气的“海洋”里。科学家很早就开始了对空气的研究。
(1)空气主要由 和氧气组成,它们的体积比约为 。
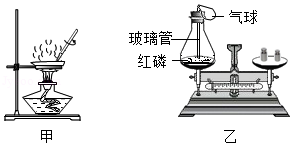
(2)实验室中可用图I所示的装置粗略研究空气的组成。反应的文字表达式是 , 红磷燃烧的主要现象为 。
(3)实验结束后此同学发现自己测定的氧气体积分数偏低,你认为造成该误差的可能原因是:(写出两条即可)
① 。② 。
(4)不能用木炭代替红磷进行上述实验的原因是 。
(5)200年前,拉瓦锡用图II所示的装置研究了空气的组成。他把少量汞放在密闭的容器中连续加热,得到了红色的氧化汞粉末,同时钟罩内的汞液面上升。该化学反应的文字表达式是 。汞液面上升的原因是 。
(6)空气在标准状况下的密度是1.29 g/L,以下四种气体中只能用排空气法收集的是 ,既能用排水法收集,又能用向下排空气法收集的是 。
| 气体 |
A |
B |
C |
D |
| 标准状况下密度(g/L) |
1.997 |
1.429 |
0.771 |
0.717 |
| 在水中的溶解性 |
可溶 |
不易溶 |
易溶 |
难溶 |
根据如图所示的实验回答问题。
(1)甲为蒸发溶液的实验。加热时若不搅拌,造成的后果是 ;当观察到 时,停止加热。
(2)乙为通过红磷燃烧前后质量的测定验证质量守恒定律的实验。用红热的玻璃管引燃红磷,实验现象是:红磷燃烧,产生 ,放出大量热。实验中气球的作用除了使装置密闭之外,还可以防止 ;实验时若取用红磷的量不足,对实验的结果 (选填“有”或“没有”)影响。
理化知识在生产,生活中有广泛的应用。
(1)空气中能供给呼吸的气体是 。
(2)幼儿及青少年缺 元素会患佝偻病和发育不良。
(3)冰箱中放入活性炭除异味,利用了活性炭的 性。
(4)打开汽水瓶盖,有气泡冒出,说明气体溶解度随压强减小而 。
(5)纯棉、涤纶和聚酯纤维三种布料中, 的吸水性和透气性较好。
用天然气热水器(如图所示)将质量为40kg,温度为15℃的水加热到40℃,完全燃烧了0.15m3的天然气。
(1)天然气的主要成分为CH4.CH4完全燃烧的化学方程式为: 。
(2)水需吸收 J的热量。
(3)热水器的效率为 %[水的比热容是4.2×103J(kg•℃)、天然气的热值是3.5×107J/m3)。

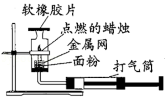
如图所示为粉尘爆炸的实验装置。用打气筒向容器内打气吹散面粉,瞬间发生爆炸,软橡胶片被冲飞,蜡烛熄灭。
(1)吹散面粉的目的是增大 的接触面积。
(2)软橡胶片被冲飞时内能转化为 。
(3)蜡烛熄灭的原因是 。
小明怀疑自家菜地因施用硫酸铵出现了较为严重的土壤酸化问题,于是和化学兴趣小组的同学对此进行了探究。
[查阅产品说明]小明同学根据图1所示产品说明书中的 和硫酸铵的组成,推测硫酸铵受热可能会分解生成氨气,使肥效降低。
[探究1]土壤的酸碱性
实验1:按图2所示溶解土样,玻璃棒搅拌的目的是 ;用pH试纸测量土样浸出液的pH约为4,说明土壤呈酸性。
[探究II]硫酸铵具有哪些性质
实验2:25℃时,将30g硫酸铵加入50g水中,完全溶解,此时所得溶液对应图3中 (选填序号)点的状态,测得其pH约为5。
实验3:为证明硫酸铵受热分解生成了氨气,小组同学进行了图4所示的实验,观察到的实验现象为:①硫酸铵固体减少;②用酚酞溶液浸湿的滤纸 。③小气球变大。
小明依据现象①和②,小红只依据③,都得出了“硫酸铵受热分解”的结论。小组同学认为小红的依据不合理,小气球胀大可能是装置中的空气受热膨胀所致。若要通过小气球的变化得出“硫酸铵受热分解”的结论,还需继续进行观察,若 ,才能得出这一结论。
实验4:按图5所示进行实验,闻到刺激性气味,说明硫酸铵能与熟石灰发生反应。
[拓展应用]
(1)为保证铵态氮肥的肥效,不能高温暴晒,不能 。
(2)硫酸铵中氮元素被植物吸收后,剩余的硫酸使得土壤酸化,可用熟石灰进行改良,反应的化学方程式为 。
