下图为甲、乙两种固体物质的溶解度曲线。
⑴溶解度随温度升高而增大的物质是 (填“甲”或“乙”);
⑵某同学在t1℃时进行如图2实验,充分搅拌得到相应的液体①一③。①一③形成的溶液中属于饱和溶液的是 (填序号);
⑶在溶液③中再加入25g甲,充分搅拌,所得溶液中溶质的质量分数为 (精确到0.1%)。
⑷若固体甲中含少量固体乙,在提纯固体甲时一定要用到的玻璃仪器有 ;
⑸若甲为KNO3,如图3所示,20℃时,将盛有饱和KNO3溶液
的小试管放入盛水的烧杯中,向烧杯中加入某物质后,试管中
有晶体析出。加入的物质可能是下列中的 (填字母序号)。
A氢氧化钠固体 B生石灰固体 C冰块
D硝酸铵固体 E.浓硫酸
化工生产中为了加快反应速率,常常先把反应的固体配成溶液再两两混合。
(1)在农业上,为了合理使用农药,常把不溶于水的固体或液体农药配成 _________ 或 _________ ,用来喷洒受病虫害的农作物。
(2)用X射线检查肠胃病时,医生会让病人服用“钡餐”来辅助检查,“钡餐”就是
硫酸钡(溶液、悬浊液、乳浊液)。
指出下列溶液中的溶质和溶剂,将其填入下表中.
| 溶液 |
溶质 |
溶剂 |
| (1)生理盐水 |
||
| (2)澄清的石灰水 |
||
| (3)碘酒 |
||
| (4)稀盐酸(氯化氢气体的水溶液) |
||
| (5)高锰酸钾溶液 |
||
| (6)酒精溶液 |
溶液是由一种或几种物质分散到另一种物质里,形成的________而________的混合物.能溶解其他物质的物质叫做________,被溶解的物质叫做________.溶液由________在________里溶解而成.如碘酒中碘是________,酒精是________.固体、气体溶于液体时,________是溶质,________是溶剂.两种液体相互溶解时,通常把量多的一种叫做________;当其他液体和水相互溶解时,通常都习惯把水看作溶剂.通常没有指明溶剂的溶液,一般是指________.水是最重要的溶剂,但却不是唯一的溶剂.
在如图所示装置的试管中,加入硝酸铵固体,片刻后,U型管中左侧液面将 _________ (填“上升”、“下降”或“不变”),产生这一现象的原因是 ______ ___。若加入 _________ 固体,现象则相反。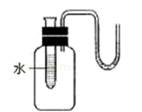
学习溶液的知识后,可以帮助我们正确认识溶液的组成及物质的溶解过程,下表是几位同学对溶液的错误认识,请你用熟悉的实例来否定其观点.
| 序号 |
错误观点 |
否定实例 |
| (1) |
溶液一定是无色的 |
|
| (2) |
均一、稳定的液体一定是溶液 |
|
| (3) |
溶液中的溶剂一定是水 |
|
| (4) |
一种溶剂最多溶解一种溶质 |
|
| (5) |
两种液体混合后充分振荡,一定得到溶液 |