(某纯碱样品中混有少量的氯化钠,为了测定该样品中碳酸钠的质量分数,小明同学准确称取 12.0g样品,做了如下实验: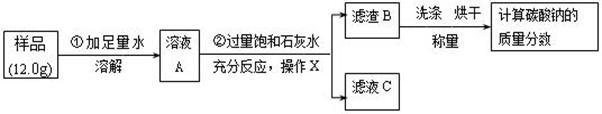
请回答下列问题:
(1)操作X用到的玻璃仪器除烧杯、玻璃棒外,还必需有 。
(2)滤液 C中的溶质是 ,若向滤液 C中滴加稀盐酸,写出过程中发生的一个中和反应的化学方程式 。
(3)若将滤渣B洗涤烘干后,称量其质量为 10.0g , 计算纯碱样品中的 Na2CO3的质量分数是多少?(结果保留一位小数,要求写出计算过程)
【2015年广东省佛山市】某腐蚀印刷电路板的废液中含有CuCl2和FeCl2,为了分析该废液的组成,取1000g废液,设计如下实验方案进行探究:
实验过程中加入废铁屑的质量、析出Cu的质量的数据记录如下表:
| 废铁屑的质量/g |
20 |
40 |
60 |
80 |
| 析出Cu的质量/g |
12.8 |
25.6 |
32 |
32 |
(注:废铁屑中的杂质不溶于废液也不与废液反应,不考虑过滤中的损失。)
(1)1000g废液与足量废铁屑完全反应,析出Cu的质量为 。
(2)废铁屑中单质Fe的质量分数为 。
(3)计算1000g废液中CuCl2的质量分数。(写出计算过程,结果保留小数点后一位)
(4)1000g废液中FeCl2的质量分数为 。(结果保留小数点后一位)
【2015年甘肃省武威市、白银市、定西市、酒泉市、临夏州】某补钙剂说明书的部分信息如右下图所示。现将有20片该药剂制成的粉末与40g盐酸混合(其他成分不与盐酸反应),恰好完全反应后称得剩余物的质量为55.6g。
(1)青少年缺钙出现的疾病是 。
(2)该品牌补钙剂每片含的CaCO3质量为多少?
(3)该盐酸中溶质的质量分数是多少?(精确到0.1%)。
【2015年甘肃省兰州市】现有家庭食用碱样品12g(主要成分Na2CO3,其它成分不与酸反应),向其中加入某未知浓度的盐酸,生成气体的质量与加入盐酸的质量
关系如图。请计算: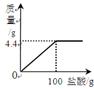
(1)食用碱中碳酸钠的纯度是多少?
(2)盐酸的溶质的质量分数是多少?(要求写出计算过程,结果精确到0.1)
【2015年广西省南宁市】为测定某纯碱样品(含少量硫酸钠杂质)中碳酸钠的质量分数,某化学兴趣小组进行以下实验,取一定质量的样品放置于烧杯中,向烧杯中滴加一定溶质质量分数的稀盐酸,实验测得烧杯中物质的总质量与加入稀盐酸的质量的关系如右下图所示。求: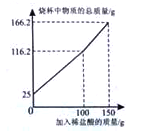
(1)所取样品的质量是 g。
(2)样品中碳酸钠的质量分数是 (精确到0.1%)。
(3)所用稀盐酸的溶质质量分数(写出具体的计算过程)。
【2015年湖北省十堰市】某样品由氧化铜和铜组成。取10.0g该样品于烧杯中,向其中加入192.0g某浓度的稀硫酸,恰好完全反应,最终所得溶液质量为200.0g。(已知:CuO+H2SO4=CuSO4+H20)
(1)所取样品中含铜元素的质量为 g.
(2)计算最终所得溶液中溶质的质量分数。(请写出计算过程)