(14分)
含硫化合物在工业生产中有广泛的用途。
(1)对于可逆反应2SO2(g)+O2(g) 2SO3(g) △H<0,下列研究目的和图示相符的是
2SO3(g) △H<0,下列研究目的和图示相符的是
(填序号)
| 序号 |
A |
B |
C |
D |
| 目的 |
压强对平衡的影响 |
温度对转化率的影响 |
增加O2浓度对速率的影响 |
浓度对平衡常数的影响 |
| 图示 |
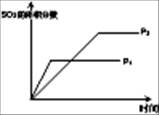 |
 |
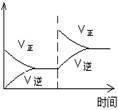 |
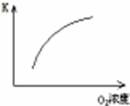 |
(2)在5000C有催化剂存在的条件下,向容积为2L的甲乙两个密闭容器中均充入2molSO2和1molO2。甲保持容积不变,乙保持压强不变,充分反应后,均达平衡状态,此时SO3的体积分数甲
乙。(填“>”“<”或“="”" )
(3)向2L的甲容器中充入2molSO2、1molO2,测得SO2的平衡转化率与温度的关系如下图所示。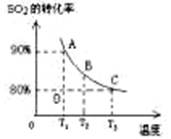
Ⅰ.在T1温度下,反应进行到状态D时,v正 v逆。(填“>”“<”或“="”" )
Ⅱ.T3温度下,平衡时测得反应放出的热量为Q1,在相同温度下若再向容器中通入2molSO2、1molO2,重新达到平衡,测得反应又放出热量Q2 。则下列说法中正确的是 。(填序号)
A.相同温度下新平衡时容器中的压强是原平衡时的两倍
B.Q2一定大于Q1
C.新平衡时SO2的转化率一定大于80%
(4)在甲容器中充入一定量的SO2和1.100molO2,在催化剂作用下加热,当气体的物质的量减少0.315mol时反应达到平衡,此时测得气体压强为反应前的82.5%,则SO2的转化率为 。
(5)若用氢氧化钠溶液吸收SO2气体恰好得到酸式盐,已知该酸式盐溶液呈弱酸性,则溶液中各离子浓度由大到小的顺序为 。(用离子浓度符号表示)
(6)一定温度下,用水吸收SO2气体,若得到pH=5的H2SO3溶液,则溶液中亚硫酸氢根离子和亚硫酸根离子的物质的量浓度之比为 。(已知该温度下H2SO3的电离常数:Ka1=1.0×10-2mol/L,Ka2=6.0×10-3mol/L)
完成下列方程式:
①与水的反应
②钠与硫酸铜溶液反应
③过氧化钠与CO2的反应
④Cl2与水的反应
有一种固体混合物,可能是由KNO3,K2SO4,KCl,CuCl2,CaCl2,和Na2CO3中的一种或几种组成,为了鉴别他们进行以下试验:
(1)将固体混合物溶于水,搅拌得无色透明溶液
(2)在此溶液中加入BaCl2溶液产生白色沉淀,过滤
(3)向上诉沉淀中加入足量的稀盐酸,沉淀全部消失。
(4)取(3)中滤液,滴加AgNO3有白色沉淀产生,且不溶于稀硝酸
推断:固体混合物中肯定含有
肯定没有
但不能判断出是否含有
在下列物质
| A.:烧碱, | B.NH3.H2O, |
| C.SO3, | D.铁片,(E)食盐水,(F)甲烷, |
(G)醋酸,(H)碳酸钙中,
属于电解质的是____________,其中属于强电解质的是___,
既不属于电解质又不属于非电解质___________ 。
从铁、盐酸、氧气、水、硝酸银溶液五种物质中选出一种或两种作反应物,按下列要求的反应类型各写一个化学方程式
(1)化合反应___________________________________
(2)分解反应___________________________________
(3)置换反应___________________________________
(4)分解反应___________________________________
下列物质:①H2O ②NaCl ③H2SO4 ④Ca(OH)2 ⑤Fe3O4 ⑥CuSO4·5H2O ⑦HNO3 ⑧AgNO3 ⑨NaHCO3 其中属于氧化物的是_____________,属于碱的是_______属于酸的是_________,属于盐的是___________