下列各示意图与对应的表述正确的是: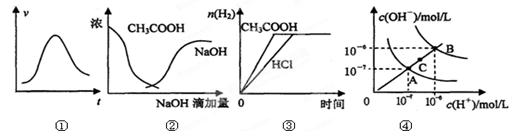
| A.图①表示一定条件下某化学反应的速率随时间变化的趋势图,该反应一定为放热反应 |
| B.图②中曲线表示将氢氧化钠溶液滴加到醋酸溶液浓度的变化趋势图 |
| C.图③表示等体积、等物质的量浓度的盐酸和醋酸,分别加足量镁粉,产生H2的物质的量的变化 |
| D.图④为水的电离平衡曲线图,若从A点到C点,可采用在水中加入适量NaOH固体的方法 |
在化学学科中,经常使用下列物理量,其中跟阿伏加德罗常数(NA)均无关的组合是:
①相对原子质量(Mr)②摩尔质量(M)③原子半径(r)④物质的量(n)⑤气体摩尔体积(Vm)⑥溶解度(S)⑦溶质的质量分数(W)
| A.①③⑥⑦ | B.②④⑤⑥ | C.①②③⑤ | D.②③⑤⑥⑦ |
某工厂排出的废液中含有Ba2+、Ag+、Cu2+,用①Na2SO4溶液,②NaOH溶液,③盐酸三种试剂将它们逐一沉淀并加以分离,加入试剂的正确顺序是:
| A.②③① | B.②①③ | C.①②③ | D.③①② |
某溶液中只含Na+、Mg2+、SO42-、Cl-,其物质的量浓度比为Na+∶Mg2+∶Cl-=3∶5∶5,若Na+的浓度为3 mol/L,则SO42-的浓度为:
| A.2 mol/L | B.3 mol/L | C.4 mol/L | D.8 mol/L |
欲使1L 0.5mol/L的NaOH溶液的浓度增大一倍,可采取的合理措施是:
| A.加入20g 固体NaOH,搅拌、溶解 |
| B.将溶液加热浓缩至0.2L |
| C.加入10mol/L的NaOH溶液0.1 L,再稀释至1.5 L |
| D.加入1 L 1.5 mol/L的NaOH溶液混合均匀 |
配制一定浓度的NaOH溶液时,下列操作使所配溶液浓度偏低的有几个:
①容量瓶中的原有蒸馏水未除去
②溶解用的烧杯未经洗涤
③定容时观察液面俯视
④用胶头滴管向容量瓶加水时,水未到刻度线即停止加水
⑤所用的NaOH中混有Na2CO3
⑥用托盘天平称取一定质量的NaOH时,所用的小烧杯内壁不太干燥
⑦NaOH在烧杯中溶解后立即将溶液转移到容量瓶内
| A.1 | B.2 | C.3 | D.4 |