美日科学家因研发“有机合成中的钯催化的交叉偶联”而获得2010年度诺贝尔化学奖。有机合成常用的钯/活性炭催化剂长期使用,催化剂会被杂质(如:铁、有机物等)污染而失去活性,成为废催化剂,故需对其回收再利用。一种由废催化剂制取氯化钯(PdCl2)的工艺流程如下:
(1)甲酸还原氧化钯的化学方程式为 。
(2)加浓氨水时,钯元素转变为可溶性[Pd(NH3)4]2+,此时铁元素的存在形式是 (写化学式)。
(3)王水是浓硝酸与浓盐酸按体积比1∶3混合而成的,钯在王水中溶解的过程中有化合物A和一种无色、有毒气体B生成。
①气体B的化学式为
②经测定,化合物A由3种元素组成,有关元素的质量分数为Pd:42.4%,H:0.8%。则A的化学式为 ;
(4)钯的回收率高低主要取决于王水溶解的操作条件,已知反应温度、反应时间和王水用量对钯回收率的影响如图1~图3所示,则王水溶解钯的适宜条件是:反应温度为 ,反应时间约为 ,含钯的样品与王水的质量比为 。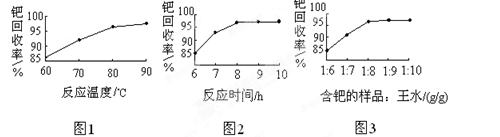
(5)700℃“焙烧1”的目的是 , 550℃“焙烧2”的目的是 。
(12分)实验室里需要纯净的氯化钠溶液,但手边只有混有硫酸钠、碳酸氢铵的氯化钠。某学生设计了如下方案: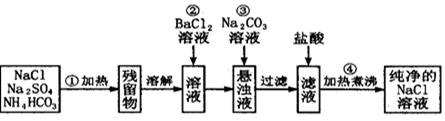
如果此方案正确,那么:
(1)操作①可选择_____仪器。
| A.烧瓶 | B.烧杯 | C.锥形瓶 | D.坩埚 E、蒸发皿 |
(2)操作②是否可改为加硝酸钡溶液?为什么?(填能或不能)理由
(3)进行操作②后,如何判断SO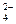 已除尽,方法是__________
已除尽,方法是__________
(4)操作③的目的是_________
为什么不先过滤后加碳酸钠溶液?理由是___________________。
(5)操作④的目的是____________________。
Ⅰ⑴用14.2g无水硫酸钠配制成500 ml溶液,其物质的量浓度为▲mol/L。
⑵若从上述溶液中取出10 ml,则这10 ml 溶液的物质的量浓度为▲mol/L,含溶质的质量为▲g。
⑶若将上述10 ml 溶液用水稀释到100 ml,所得溶液中Na+的物质的量浓度为▲mol/L;若将稀释后溶液中的SO42-全部沉淀下来,至少需要加入0.1 mol/L的BaCL2溶液
▲ml 。
Ⅱ现有36%的醋酸(CH3COOH),密度为1.04g/ml.,
欲配制0.1 mol/L的醋酸250 ml,需要取用36%的醋酸▲ml。
需要使用的实验仪器有烧杯、▲、▲、▲、▲,
若配制时仅有其中一步操作(如图所示)有错误,其他操作全部正确,则所配醋酸的浓度 ▲(填“正确”、“偏大”或“偏小”)。
▲(填“正确”、“偏大”或“偏小”)。
在实验室里制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫,为了检验SO2和C2H4的性质,有人设计下列实验方案。
(1)I、II、III、IV装置可盛放的试剂是I▲;II▲;III▲;IV▲(将下列有关试剂的序号填入空格内);
| A.品红溶液 | B.NaOH溶液 |
| C.浓H2SO4 | D.酸性KMnO4溶液 |
(2)能说明SO2气体存在的现象是▲;
(3)使用装置II的目的是▲;
(4)确定含有乙烯的现象是▲。
(5)如果Ⅳ盛放的溶液为溴水,那么发生的化学方程式为▲,反应类型为▲
如下图所示的装置中,A是氯气发生装置,C、D 为气体净化装置(C中装有饱和食盐水;D 中装有浓硫酸),E 是硬质玻璃管装有细铁丝网,F为干燥的空广口瓶,烧杯G 中装有氢氧化钠溶液。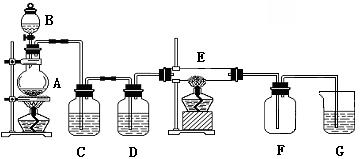
试回答:
(1)实验室制氯气的化学方程式:_______________________________;
(2)C装置的作用是________________;D 装置的作用是__________________;
E中发生化学反应的方程式为:_____________________________。
(3)烧杯G 中装有氢氧化钠溶液的作用是___________________;发生反应的化学方程式为:_______________________________________。
在酸碱中和滴定的操作中,用标准溶液润洗滴定管2—3次的目的是。判断滴定终点的现象是。若先用待测溶液润洗锥形瓶,则对滴定管结果的影响是。