曾经有一种固氮的方法:1100°C通N2和CaC2反应得到CaCN2 。
已知:CaCN2+3H2O = 2NH3+CaCO3;CaC2+2H2O = C2H2↑+Ca(OH)2
(1)某同学采用以下装置(加热和夹持仪器已略去)制取少量的CaCN2
①U形管中盛放的物质是 (填一种);
② (填“能”或“不能”)用普通玻璃管代替图中石英管;
(2)检验反应后的固体(用W表示)中含有氮元素该同学将适量W溶于水,有气泡产生,说明固体中含有氮元素,该结论不正确。若要得出正确结论,还需进行的实验是 。
(3)测定W中CaCN2的质量分数
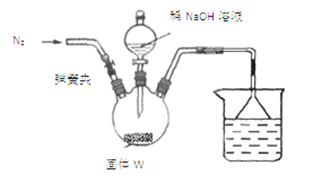
步骤Ⅰ:按如图所示装置(夹持仪器已略去)进行实验:关闭弹簧夹,将漏斗中溶液逐滴加入到三颈瓶中,当W反应完全后,打开弹簧夹,通入氮气,直至氨气被200mL0.1 mol·L-1硫酸完全吸收。
步骤Ⅱ:准确量取烧杯中溶液20.00mL置于锥形瓶中,滴入几滴指示剂,用cmol·L-1NaOH溶液滴定过量的硫酸,实验测得消耗标准溶液的平均体积为vmL。
已知三种常用指示剂变色pH范围如下:
| 指示剂 |
a |
b |
c |
| 变色pH范围 |
3.1~4.4 |
8.0~10.0 |
4.4~6.2 |
| 说明 |
pH<3.1显红色 pH>4.4显黄色 |
pH<8.0显无色 pH>10.0显红色 |
pH<4.4显红色 pH>6.2显黄色 |
①上述滴定过程中,不宜选用的指示剂是 (填字母序号);
②烧杯中最终吸收氨气的物质的量为 mol;经进一步计算可求得W中CaCN2质量分数。
③上述实验所得结果明显偏小,若不考虑装置的气密性和操作误差,则导致结果偏小的可能原因是
(写1种)。
写出下列制取氯气的化学反应方程式:
(1)实验室用二氧化锰跟浓盐酸反应制取氯气的化学反应方程式为_____________________。
(2)高锰酸钾(KMnO4)是常用的氧化剂,在酸性条件下, 被还原成Mn2+。试写出用高锰酸钾跟浓盐酸在室温下制取氯气的化学反应方程式:____________________________。
被还原成Mn2+。试写出用高锰酸钾跟浓盐酸在室温下制取氯气的化学反应方程式:____________________________。
(3)历史上曾用“地康法”制取氯气,这一方法是用CuCl2作催化剂,在450 ℃时利用空气中氧气跟氯化氢反应制取氯气,化学反应方程式为__________________________。
从氯元素化合价的变化来看,以上三种方法的共同点是____________,比较以上三个反应,可得出三种氧化剂的氧化能力由强到弱的顺序为____________。
海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如下:
(1)指出取提碘的过程中有关的实验操作名称:①______;②_____;写出过程②中有关反应的化学方程式______,________。
(2)提取碘过程中,可供选择的有机试剂是_______。 [ ]
| A.甲苯、酒精 |
| B.四氯化碳、苯 |
| C.汽油、乙酸 |
| D.汽油、甘油 |
(3)为使海藻灰中碘离子转化为碘的有机溶液,实验室里有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器、物品。尚缺少的玻璃仪器是_____。
醛可与NaHSO3饱和溶液发生加成反应,生成水溶性的α-羟基磺酸钠:
反应是可逆的。在通常条件下有70%~90%的原料向正反应方向转化。
(1)若氯苯中含有杂质苯甲醛,要除去此杂质,可作用的试剂是____,反应的化学方程式为:____;分离的方法是____。
(2)若使CH3—CHOH—SO3Na转化为乙醛,可采用的试剂是____,反应的化学方程式为____,分离的方法是____。
甲、乙、丙三位同学设计了一个实验结果各自都认为自己的试样中含有SO42-离子。甲的实验为:
(1)乙认为甲的实验不严谨,因为试样A中若含有____离子(仅填一种),也会有此现象。乙的实验为:
(2)丙认为乙的实验也不严谨,因为试样B中若含有____(仅填一种),也会有此现象。丙的实验</PGN0055B.TXT/PGN>为:
若丙方案合理,则回答:
(3)其中试剂Ⅰ是____,现象Ⅰ是____。
试剂Ⅱ是____,现象Ⅱ是____。(若你认为丙方案不合理,以上回答可以不填)。
某化学课外小组所做实验的示意图如图所示。
图中“→”表示气体流向,M是一种纯净而干燥的气体,Y为另一种气体,E内有棕色气体产生。
实验所用的物质,只能由下列物质中选取:Na2CO3、Na2O2、NaCl、Na2O、CaCl2、(NH4)2CO3、碱石灰等固体及蒸馏水。
据此实验,完成下列填空:
(1)A中所用装置的主要仪器有____。
(2)B中所选的干燥剂是____,其作用是____。
(3)C中发生的主要反应的化学方程式是____。
(4)制取Y气体的D装置所用的主要仪器是____,制取Y气体的化学方程式是____。
(5)当F中充有一定量气体后,D停止送气,A停止加热,并立即关闭两个活塞,这时若将F汉入冰水中,可看到F中的现象是____,其原因是____。