H2O2是一种强氧化剂,被广泛应用于水处理及卫生消毒等方面。
(1)H2O2不稳定,当其中含Fe2+时,会发生反应:
 ,则Fe2+在此过程中所起的作用是______________,当生成336mL O2(标准状况)时,反应中转移电子的物质的量为_______mol。
,则Fe2+在此过程中所起的作用是______________,当生成336mL O2(标准状况)时,反应中转移电子的物质的量为_______mol。
(2)下表是在常压、60℃和不同pH条件下,6mL30% H2O2在60min内释放出氧气的体积。则下列说法正确的是___________。
a.pH越大,H2O2的分解速率越大
b.pH在9左右,H2O2的分解速率最大
c.6mL 30% H2O2分解最多释放出的氧气的体积为639mL
d. pH=5.50时,0~60min内,v(O2)=1.5mL
(3)溶液中H2O2的残留量可用一定浓度的酸性KMnO4溶液来测定,反应中MnO4-
被还原为Mn2+,该反应的离子方程式为______________。
(4)科学工作者以Ir-Ru/Ti为阳极、ACFC为阴极,在酸性环境、不断通入空气的条件下直接电解水来制备H2O2。电解过程中,阳极区溶液的pH_ (填“增大”“不变”或“减小”),阴极产生H2O2的电极反应式为_______。若不通空气,则阴极得到的产物是_______ 。
(5)己知断裂1mol化学键所需的能量
143,H-O为463。则 .
.
(1)某学生欲用铁片与2mol·L-1盐酸反应来制取少量氢气,现欲提高化学反应速率,实验中可采用①;②;③_________等方法;(2)碳酸钠溶液与盐酸的反应若欲降低化学反应速率可采取的方法有①;②________________________。
下列3种有机化合物A:CH2=CH2、 B: 、 C:CH3COOH
、 C:CH3COOH
(1)写出化合物A、C中的官能团、。
(2)能使溴的四氯化碳溶液褪色反应的化学方程式为:,
该反应类型为:。
(3)能与乙醇发生酯化反应的化学方程式为:,
(4) 在浓硫酸作用下,与浓硝酸反应的反应类型为:。
在浓硫酸作用下,与浓硝酸反应的反应类型为:。
下表是元素周期表中短周期元素部分,表中字母分别代表一种元素:
| a |
b |
||||||
| d |
e |
f |
|||||
| c |
g |
h |
(1)上述 元素(填元素名称)可以形成硬度最大的单质。
(2)“神舟”六号飞船内需要有一种化合物来吸收宇航员呼出的 CO2,并释放出O2,你认为该
物质应该是由上表中的 和 元素(填元素名称)组成的。飞船中需要制造一种适合宇航员生存的人工生态环境,应该在氧气中充入一种气体用于稀释氧气,该气体分子是 。
(3)表中元素g的氢化物稳定性比元素e的氢化物的稳定性 (填“强”或“弱”)。
(4)将潮湿的由h元素构成的单质通过甲装置后,再通过放有干燥红色布条的乙装置,红色布条不褪色。则甲装置中所盛试剂可能是
|
①浓硫酸②NaOH溶液③KI溶液④饱和食盐水
(5)写出h元素构成的单质与水反应的化学方程式: 。在原子序数1—18号元素中,按要求用合适的化学用语填空:
(1)与水反应最剧烈的金属是_____________。
(2)与水反应最剧烈的非金属单质是_____________。
(3)原子半径最小的元素是______________。
(4)最稳定气态氢化物的化学式是______________。
(5)最高价氧化物对应水化物的酸性最强的化学式是_______________。
(6)电子数为10的化合物分子式__、__、__、__。
(共10分)有下列各组物质:
| A.O2和O3(臭氧) |
B. 和 和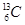 |
C.CH3CH2CH2CH3和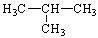 |
D.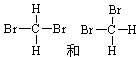 |
E.甲烷和庚烷
F.(CH3)2CH2与C(CH3)4
G.金刚石和石墨
H.液氯与氯气
(1)组两物质互为同位素(2)组两物质互为同素异形体
(3)组两物质属于同系物(4)组两组物质互为同分异构体
(5)组中的物质是同一物质