硫酸、盐酸和硝酸并称为工业上的“三大酸”,实验室中也常用三大酸制取某些气体,制取、收集及尾气处理装置如图所示(省略加热装置、夹持和净化装置)。仅用此装置和表中提供的部分物质完成相关实验。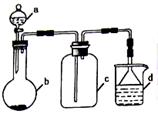
| 序号 |
a中的物质 |
b中的物质 |
c中收集的气体 |
d中的物质 |
| 甲 |
浓硫酸 |
Na2SO3 |
① |
② |
| 乙 |
浓硝酸 |
Cu |
③ |
NaOH |
| 丙 |
浓盐酸 |
MnO2 |
Cl2 |
NaOH溶液 |
按要求回答下列问题:
(1)表格中①②③三种物质分别是__________、__________、________(填化学式)。
(2)实验乙中生成气体③的离子反应方程式为________________________;某同学认为将浓硝酸改为稀硝酸,即可以利用本套装置制取NO气体,该同学的设计________(填“正确”或“不正确”)。
(3)已知实验丙中生成氯气的化学方程式为4HCl(浓)+MnO2  MnCl2+ Cl2↑+2H2O,在该反应中每生成22.4L(标准状况下)氯气,被氧化HCl的物质的量为__________,转移电子的物质的量为________;d装置中发生反应的离子方程式为_________________。实验室还可以用高锰酸钾和浓盐酸反应制取氯气,完成并配平该反应的离子方程式:
MnCl2+ Cl2↑+2H2O,在该反应中每生成22.4L(标准状况下)氯气,被氧化HCl的物质的量为__________,转移电子的物质的量为________;d装置中发生反应的离子方程式为_________________。实验室还可以用高锰酸钾和浓盐酸反应制取氯气,完成并配平该反应的离子方程式:
____ MnO4-+ ____ H+ + ____ Cl- ____ Mn2+ + ____ Cl2↑+ ____ _________
____ Mn2+ + ____ Cl2↑+ ____ _________
按要求完成下列填空
(l)写出下列物质的电离方程式:
Fe2(SO4)3__________________________________________________,
NaHCO3______________________________________________________。
(2)写出下列反应的离子方程式:
稀盐酸与碳酸钙反应____________________________________________,
氢氧化钡溶液与稀硫酸反应_______________________________________。
(3)写出与下列离子方程式相对应的化学方程式:
H++OH-=H2O __________________________________________,
CO32-+2H+=CO2↑+H2O__________________________________。
(1)同温同压下,同体积的NH3和H2S气体的质量比是___________;同质量的NH3和H2S气体的体积比是__________;同质量的NH3和H2S气体中所含氢原子个数比是___________;若两者所含氢原子个数相等,它们的物质的量比是________。
(2)Na2SO4••10H2O的摩尔质量是__________,483gNa2SO4••10H2O中所含Na2SO4••10H2O的物质的量是_______,所含Na+的物质的量是_________,所含H2O分子的数目是_______个。
在有机物分子中,不同位置的氢原子的核磁共振谱中给出的特征峰值(信号)也不同,根据峰值(信号)可以确定有机物分子中氢原子的种类和数目。
(1)下列有机物分子中,其核磁共振氢谱图中只有1个峰的物质是________。
| A.CH3—CH3 | B.CH3COOH | C.CH3COOCH3 | D.CH3COCH3 |
(2)化合物A和B的分子式都是C2H4Br2,A的核磁共振氢谱图如下所示,则A的结构简式为________。请预测B的核磁共振氢谱图上有________个峰。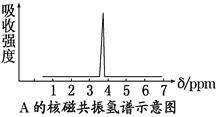
写出下列反应的化学方程式
(1) 苯的硝化反应
(2) 实验室制取乙烯
(3)乙烯与溴水反应
(4)乙烯发生加聚反应
用系统命法写出下列物质名称或结构简式
(1)2,2,3-三甲基丁烷的结构简式是
(2)1,3-丁二烯的结构简式是
(3) 的系统命名是:
的系统命名是:
(4) 的系统命名是
的系统命名是