下图甲是CO2电催化还原为碳氢化合物的工作原理示意图,用一种钾盐水溶液作电解液;图乙是用H2还原CO2制备甲醇的工作原理示意图,硫酸为电解质溶液。下列说法不正确的是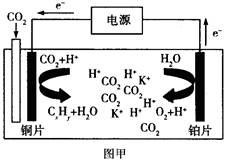
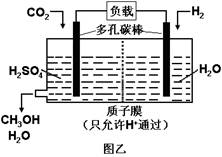
| A.甲中铜片作阴极,K+向铜片电极移动 |
| B.乙中正极发生的电极反应为CO2+6e-+6H+=CH3OH+H2O |
| C.甲中若CxHy为C2H4,则生成1 mol C2H4的同时生成2 molO2 |
| D.乙中H2SO4的作用是增强溶液的导电性 |
下图表示M的结构简式,下列有关M的说法正确的是
| A.M可以发生加成、加聚、水解、酯化等反应 |
| B.l mol M最多可以与3 mol NaOH反应 |
| C.M苯环上的一氯取代物有两种不同结构 |
| D.l molM最多可以与5 mol H2发生加成反应 |
下列各表述与下图所示一致的是
| A.图1表示某吸热反应t1时刻升高温度时,正逆反应速率的变化 |
| B.图2表示某放热反应过程的能量变化,若使用催化剂,a点会降低 |
C.图3表示向含等物质的量的NaOH、Na2CO3混合溶液中滴加0.1 mol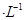 盐酸至过量时,产生气体的体积与消耗盐酸的关系 盐酸至过量时,产生气体的体积与消耗盐酸的关系 |
| D.图4表示Cl2通入H2SO3溶液中pH的变化 |
下列实验过程中,始终看不到明显变化的是
| A.向l0mL0. 1mol·L-1FeI2,溶液中缓缓通人标准状况下11. 2mL Cl2 |
| B.向AlCl3溶液中滴加Na2S溶液 |
| C.向含有Na+、Fe2+、Cl-、SO42-离子的溶液中通入NO2 |
| D.向5mL0.1mol·L-1NaOH溶液中,逐滴加入1 mL0.1 mol·L-1AlCl3溶液,边滴加边振荡 |
X、Y、Z、W是原子序数依次增大的四种短周期元素,X的最高价氧化物对应的水化物的化学式为H2XO3,Y的最外层电子数是电子层数的3倍,Z是地壳中含量最高的金属元素,W的一种核素的质量数为28,中子数为14。下列说法正确的是
| A.原子半径由大到小的顺序是Z>W>Y>X |
| B.元素的非金属性W>Y>X |
| C.Z2Y3、WX分别是离子化合物、共价化合物 |
| D.X、Z、W的最高价氧化物都是酸性氧化物 |
下列实验操作、现象和结论均正确的是
| 选项 |
实验操作 |
现象 |
结论 |
| A |
CH2=CH2通入溴的四氯化碳溶液中 |
溶液褪色 |
CH2=CH2发生取代反应 |
| B |
KIO3溶液中加入HI溶液并加入淀粉 |
溶液变蓝色 |
氧化性:KIO3>I2 |
| C |
将盛满氯气的试管倒扣在水槽中,放在日光下静置一段时间 |
气体逐渐减少,最后变为无色 |
Cl2置换出水中的氧生成了O2 |
| D |
将苯、溴水混合后加入大试管加热 |
试管底部产生油状物 |
苯发生取代反应生成溴苯 |